题目内容
用NA表示阿伏伽德罗常数的值,下列叙述正确的是( )
| A、1mol金刚石中含有C-C键的数目为4NA |
| B、14克N2中含有的π键数目为NA |
| C、25℃,pH=13的NaOH溶液中含有OH-的数目为0.1NA |
| D、1L0.1mol/LAl2(SO4)3溶液中含有的Al3+总数为0.2NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.金刚石中,每个C与其它4个C原则形成4个碳碳键,根据均摊法计算出1mol金刚石中含有的碳碳键数目;
B.氮气分子中含有1个氮氮三键,双键中含有两个π键;
C.缺少氢氧化钠溶液的体积无法计算溶液中氢氧根离子的物质的量;
D.硫酸铝溶液中,铝离子部分水解,导致铝离子数目减少.
B.氮气分子中含有1个氮氮三键,双键中含有两个π键;
C.缺少氢氧化钠溶液的体积无法计算溶液中氢氧根离子的物质的量;
D.硫酸铝溶液中,铝离子部分水解,导致铝离子数目减少.
解答:
解:A.金刚石中,每个C形成的共价键为:
×4=2,则1mol金刚石形成的共价键为:1mol×2=2mol,所以1mol金刚石中含有C-C键的数目为2NA,故A错误;
B.14g氮气的物质的量为0.5mol,0.5mol氮气中含有0.5mol氮氮三键,含有π键的物质的量为:0.5mol×2=1mol,含有的π键数目为NA,故B正确;
C.没有告诉pH=13的氢氧化钠溶液的体积,无法计算溶液中氢氧根离子的物质的量及数目,故C错误;
D.1L0.1mol/LAl2(SO4)3溶液中含有溶质硫酸铝0.1mol,由于铝离子部分水解,则溶液中铝离子的物质的量小于0.2mol,Al3+总数小于0.2NA,故D错误;
故选B.
| 1 |
| 2 |
B.14g氮气的物质的量为0.5mol,0.5mol氮气中含有0.5mol氮氮三键,含有π键的物质的量为:0.5mol×2=1mol,含有的π键数目为NA,故B正确;
C.没有告诉pH=13的氢氧化钠溶液的体积,无法计算溶液中氢氧根离子的物质的量及数目,故C错误;
D.1L0.1mol/LAl2(SO4)3溶液中含有溶质硫酸铝0.1mol,由于铝离子部分水解,则溶液中铝离子的物质的量小于0.2mol,Al3+总数小于0.2NA,故D错误;
故选B.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系;有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
相关题目
网易探索2010年5月20日报道,来自法国格勒诺布尔(Grenoble)约瑟夫命傅立叶大学的研究小组发明了第一块可为人体人造器官提供电能的可植入的葡萄糖生物燃料电池,其基本原理是葡萄糖和氧气在人体中酶的作用下发生了反应,已知其总反应为:C6H12O6+6O2=6CO2+6H2O(酸性环境),则下列对该电池说法不正确的是( )
| A、消耗1mol氧气时转移4mole-,H+向正极移动 |
| B、电池负极的反应为:C6H12O6+6H2O-24e-=6CO2+24H+ |
| C、今后的研究方向是怎样提高葡萄糖生物燃料电池的效率,从而达到可以利用葡萄糖生物燃料电池为任何可植入医疗设备提供电能 |
| D、该生物燃料电池可以在高温下工作 |
关于水在人体中的作用叙述不正确的是( )
| A、将氧气运输到血液 |
| B、将体内代谢的废物通过尿液或粪便排出体外 |
| C、营养素的消化、吸收过程不需要水的作用 |
| D、通过蒸发或出汗来调节体温保持不变 |
下列实验装置不能达到预期目的是( )


| A、装置①用于测定H2O2分解的反应速率 |
| B、装置②用于证明元素的非金属性:S>C>Si |
| C、装置③用于证明Na2CO3的水解是吸热反应 |
| D、装置④用于测定中和热 |
下列实验装置或对实验现象的描述正确的是( )
A、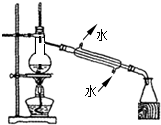 分馏装置 |
B、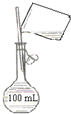 配制150 mL 0.10 mol?L-1盐酸 |
C、 烧瓶内溶液变蓝色 |
D、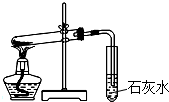 探究NaHCO3的热稳定性 |
下列仪器中,需要垫石棉网加热的是( )
A、 |
B、 |
C、 |
D、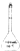 |
如图为某一工业合成简单理想的流程图,反应条件已省略.有关上述过程的说法错误的是( )

| A、物质E的化学式为C7H7NO3 |
| B、C转化为D的反应类型是还原反应 |
| C、D转化为E时,所加的反应物可以是氢氧化钠溶液和稀H2SO4 |
| D、物质A属于芳香烃 |
 喀麦隆的“杀人湖”(尼奥斯湖)曾于1986年使1800多名附近居民在一夜之间神秘死去.后经科学家考察发现,湖底有火山口,聚集了大量二氧化碳和二氧化硫等有毒气体并发现在200m深的湖底,每立方米湖水竟溶解8m3的有毒气体,目前科技人员已找到一种有效的办法将湖底的有毒气体抽出并加以处理.回答:
喀麦隆的“杀人湖”(尼奥斯湖)曾于1986年使1800多名附近居民在一夜之间神秘死去.后经科学家考察发现,湖底有火山口,聚集了大量二氧化碳和二氧化硫等有毒气体并发现在200m深的湖底,每立方米湖水竟溶解8m3的有毒气体,目前科技人员已找到一种有效的办法将湖底的有毒气体抽出并加以处理.回答: