题目内容
12.亚硝酸钠是一种工业盐,用途广泛;外观与食盐非常相似,但毒性较强.某化学兴趣小组对食盐与亚硝酸钠进行了如下探究:㈠鉴别NaCl和NaNO2
(1)测定溶液pH
用pH试纸分别测定0.1mol•L-1两种盐溶液的pH,测得NaNO2溶液呈碱性.NaNO2溶液呈碱性的原因是NO2-+H2O?HNO2+OH-(用离子方程式解释),NaNO2溶液中c(HNO2)=c(OH-)-c(H+)(用溶液中其它离子的浓度关系式表示).
(2)沉淀法
取2mL0.1mol•L-1两种盐溶液于试管中,分别滴加几滴稀硝酸银溶液,两只试管均产生白色沉淀,分别滴加几滴稀硝酸并振荡,盛NaNO2溶液的试管中沉淀溶解.该温度下Ksp(AgNO2)=2×10-8 (mol•L-1)2; Ksp(AgCl)=1.8×10-10(mol•L-1)2,则反应AgNO2(s)+Cl-(aq)═AgCl(s)+NO2-(aq)的化学平衡常数K=$\frac{1000}{9}$(计算结果写成分数).
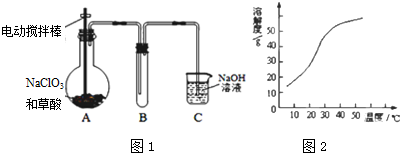
(二)实验室可用如下装置(略去部分夹持仪器)备亚硝酸钠.
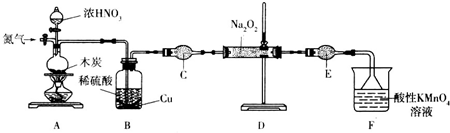
已知:①2NO+Na2O2=2NaNO2;
②酸性条件下,NO和NO2都能与MnO4-反应生成NO3-和Mn2+;Na2O2能使酸性高锰酸钾溶液褪色.
(1)加热装置A前,先通一段时间N2,目的是排出装置中的空气.
(2)装置A中发生反应的化学方程式为C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O,装置B的作用是吸收A中反应生成的二氧化氮气体,生成硝酸,与铜再反应生成一氧化氮气体.
(3)仪器C的名称为干燥管,其中盛放的药品为碱石灰(填名称).
分析 (一)(1)NaNO2溶液显示碱性,NaNO2说明为强碱弱酸盐,亚硝酸根离子水解导致溶液显示碱性;根据亚硝酸钠溶液中的质子守恒分析;
(2)写出该反应的平衡常数表达式,然后根据Ksp(AgNO2)、Ksp(AgCl)进行计算;
(二)由制备亚硝酸钠的实验装置可知,先通入氮气,将装置中的空气排出,C与浓硝酸反应生成二氧化氮、二氧化碳,B中可除去二氧化氮,C为球形干燥管,干燥NO气体,D中发生2NO+Na2O2=2NaNO2,F为尾气处理,以此来解答.
解答 解:(一)(1)由于亚硝酸钠溶液中存在水解平衡:NO2-+H2O?HNO2+OH-,所以亚硝酸钠溶液显示碱性;根据亚硝酸钠溶液中的质子守恒可得:c(OH-)=c(HNO2)+c(H+),则c(HNO2)=c(OH-)-c(H+),
故答案为:NO2-+H2O?HNO2+OH-;c(OH-)-c(H+);
(2)反应AgNO2(s)+Cl-(aq)═AgCl(s)+NO2-(aq)的化学平衡常数K=$\frac{c(N{{O}_{2}}^{-})}{c(C{l}^{-})}$,根据Ksp(AgCl)=c(Cl-)•c(Ag+)、Ksp(AgNO2)=c(NO2-)•c(Ag+)可知,K=$\frac{c(N{{O}_{2}}^{-})}{c(C{l}^{-})}$=$\frac{Ksp(AgN{O}_{2})}{Ksp(AgCl)}$=$\frac{2×1{0}^{-8}}{1.8×1{0}^{-10}}$=$\frac{1000}{9}$,
故答案为:$\frac{1000}{9}$;
(二)由制备亚硝酸钠的实验装置可知,先通入氮气,将装置中的空气排出,C与浓硝酸反应生成二氧化氮、二氧化碳,B中可除去二氧化氮,C为球形干燥管,干燥NO气体,D中发生2NO+Na2O2=2NaNO2,F为尾气处理,
(1)由上述分析可知,加热装置A前,先通一段时间N2,目的是排出装置中的空气,故答案为:排出装置中的空气;
(2)A中反应的化学方程式为:C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O,装置B的作用是吸收A中反应生成的二氧化氮气体,生成硝酸,与铜再反应生成一氧化氮气体,
故答案为:C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O;吸收A中反应生成的二氧化氮气体,生成硝酸,与铜再反应生成一氧化氮气体;
(3)仪器C的名称为干燥管,其中盛放的药品为碱石灰,
故答案为:干燥管; 碱石灰.
点评 本题考查物质的制备实验及物质鉴别,为高频考点,把握制备实验原理、实验装置作用、实验技能等为解答的关键,侧重分析与实验能力的考查,注意元素化合物知识、反应原理与实验相结合的训练,题目难度中等.

 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案①Al ②Al2O3③Al(OH)3 ④NaHSO3⑤(NH4)2CO3⑥(CH3COO)2Cu⑦NH2-CH2-COOH.
| A. | ①②③⑦ | B. | 除⑤⑥外 | C. | ②③⑦ | D. | 全部 |
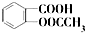 )是世界上应用最广泛的解热、镇痛和抗炎药.乙酰水杨酸受热易分解,分解温度为128℃~135℃.
)是世界上应用最广泛的解热、镇痛和抗炎药.乙酰水杨酸受热易分解,分解温度为128℃~135℃.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,反应原理如下:

制备基本操作流程如下:
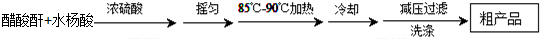
主要试剂和产品的物理常数如下表所示:
| 名称 | 相对分子质量 | 熔点或沸点(℃) | 水 |
| 水杨酸 | 138 | 158(熔点) | 微溶 |
| 醋酸酐 | 102 | 139.4(沸点) | 易水解 |
| 乙酰水杨酸 | 180 | 135(熔点) | 微溶 |
(1)制备阿司匹林时,要使用干燥的仪器的原因是醋酸酐和水易发生反应.
(2)合成阿司匹林时,最合适的加热方法是水浴加热.
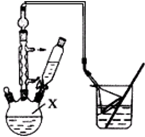
(3)提纯粗产品流程如下,加热回流装置如图:
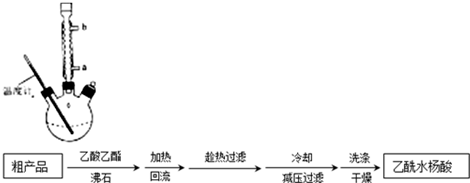
①使用温度计的目的是控制加热的温度,防止乙酰水杨酸受热易分解.
②冷凝水的流进方向是a(填“a”或“b”);
③趁热过滤的原因是防止乙酰水杨酸结晶析出.
④下列说法正确的是abc(填选项字母).
a.此种提纯方法中乙酸乙酯的作用是做溶剂
b.此种提纯粗产品的方法叫重结晶
c.根据以上提纯过程可以得出阿司匹林在乙酸乙酯中的溶解度低温时大
d.可以用紫色石蕊溶液判断产品中是否含有未反应完的水杨酸
(4)在实验中原料用量:2.0g水杨酸、5.0mL醋酸酐(ρ=1.08g/cm3),最终称得产品质量为2.2g,则所得乙酰水杨酸的产率为84.3%(用百分数表示,小数点后一位).
 水杨酸甲酯,是一种重要的有机合成原料.某化学小组用水杨酸(结构简式为
水杨酸甲酯,是一种重要的有机合成原料.某化学小组用水杨酸(结构简式为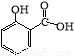 )和甲醇在酸性催化剂催化下合成水杨酸甲酯并计算其产率.
)和甲醇在酸性催化剂催化下合成水杨酸甲酯并计算其产率.实验步骤:
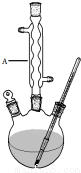
Ⅰ.如图,在三颈烧瓶中加入13.8g (0.1mol)水杨酸和24g(30mL,0.75mol)甲醇,向混合物中加入约10mL甲苯(甲苯与水形成的共沸物,沸点为85℃,该实验中加入甲苯,易将水蒸出),再小心地加入5mL浓硫酸,摇动混匀,加入1~2粒沸石,组装好实验装置,在85~95℃下恒温加热反应1.5小时:
Ⅱ.待装置冷却后,分离出甲醇,然后转移至分液漏斗,依次用少量水、5%NaHCO3溶液和水洗涤;分出的产物加入少量无水MgSO4固体,过滤得到粗酯;
Ⅲ.将粗酯进行蒸馏,收集221℃~224℃的馏分,得水杨酸甲酯9.12g.
常用物理常数:
| 名称 | 分子量 | 颜色状态 | 相对密度 | 熔点(℃) | 沸点(℃) |
| 水杨酸甲酯 | 152 | 无色液体 | 1.18 | -8.6 | 224 |
| 水杨酸 | 138 | 白色晶体 | 1.44 | 158 | 210 |
| 甲醇 | 32 | 无色液体 | 0.792 | -97 | 64.7 |
(1)仪器A的名称是球形冷凝管.
(2)实验中加入甲苯对合成水杨酸甲酯的作用是反应产生的水从反应体系中分离开来,使得平衡向右移动,同时可以减少甲醇的用量,从而提高反应的产率.
(3)实验中加入无水硫酸镁的作用是干燥剂.
(4)反应结束后,分离出甲醇采用的方法是蒸馏(填操作名称).
(5)本实验的产率为60%.
| 熔点/℃ | 沸点/℃ | |
| 1-丁醇 | -89.53 | 117.25 |
| 1-溴丁烷 | -112.4 | 101.6 |
| 丁醚 | -95.3 | 142.4 |
| 1-丁烯 | -185.3 | -6.5 |
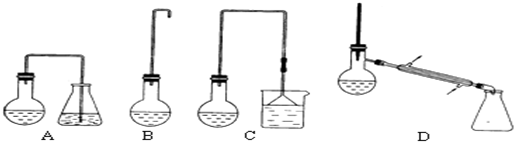
(1)制备1-溴丁烷的装置应选用上图中的C(填序号).反应加热时的温度不宜超过100℃,理由是防止1-溴丁烷因气化而逸出,影响产率且温度太高,浓硫酸氧化性增强,可能氧化溴化氢.
(2)制备操作中,加入的浓硫酸和溴化钠的作用是二者反应生成HBr.
(3)反应结束后,将反应混合物中1-溴丁烷分离出来,应选用的装置是D,(填序号);该操作应控制的温度(t)范围是101.6℃≤t<117.25℃.
(4)欲除去溴代烷中的少量杂质Br2,下列物质中最适合的是c.(填字母)
a.NaI b.NaOH c.Na2SO3 d.KCl.
 某化学实验小组想要了解市场上所售食用白醋(主要是醋酸的水溶液)的准确浓度,现从市场上买来一瓶某品牌食用白醋,在实验室中用标准NaOH溶液对其进行滴定.下表是4种常见指示剂的变色范围:
某化学实验小组想要了解市场上所售食用白醋(主要是醋酸的水溶液)的准确浓度,现从市场上买来一瓶某品牌食用白醋,在实验室中用标准NaOH溶液对其进行滴定.下表是4种常见指示剂的变色范围:| 指示剂 | 石蕊 | 甲基橙 | 甲基红 | 酚酞 |
| 变色范围(pH) | 5.0~8.0 | 3.1~4.4 | 4.4~6.2 | 8.2~10.0 |
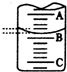
(2)如图表示50mL滴定管中液面的位置,若A与C刻度间相差1mL,A处的刻度为25,滴定管中液面读数应为25.40mL,此时滴定管中液体的体 积大于24.60ml.
(3)为了减小实验误差,该同学一共进行了三次实验,假设每次所取白醋体积均为VmL,NaOH标准液浓度为c mo1/L,三次实验结果记录如下:
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗NaOH溶液体积/mL | 26.02 | 25.35 | 25.30 |
A.实验结束时俯视滴定管中液面,读取滴定终点时NaOH溶液的体积
B.滴加NaOH溶液过快,未充分振荡,刚看到溶液变色,立刻停止滴定
C.盛装标准液的滴定管装液前用蒸馏水洗涤,未用标准液润洗
D.第一次滴定用的锥形瓶用待装液润洗过,后两次未润洗
(4)根据所给数据,写出计算该白醋中醋酸的物质的量浓度的表达式(不必化简):c(CH3COOH)=$\frac{c×(25.35+25.30)}{2V}$mol/L.
 对叔丁基苯酚(
对叔丁基苯酚(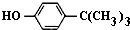 )工业用途广泛,可用于生产油溶性酚醛树脂、稳定剂和香料等.实验室以苯酚、叔丁基氯[(CH3)3CCl]等为原料制备对叔丁基苯酚.
)工业用途广泛,可用于生产油溶性酚醛树脂、稳定剂和香料等.实验室以苯酚、叔丁基氯[(CH3)3CCl]等为原料制备对叔丁基苯酚. .
.