题目内容
如图分别为NaCl、CsCl及金刚石的晶体结构模型.

(1)在NaCl晶体中,在每个Na+离子的周围与它最接近的且距离相等的Na+离子共有 个.在一个NaCl晶胞中,Cl-离子的个数等于 ,Na+离子的个数等于 .
(2)在CsCl晶体中,每个Cs+离子周围与它最接近的且距离相等的Cs+离子共有 个.每个Cs+离子周围与它最接近的且距离相等的Cl-离子共有 个.
(3)在金刚石晶体中,每个C原子周围有 个C-C键,1mol金刚石,含 C-C键 mol.
(4)如果将金刚石晶体结构模型中的C原子换成Si原子,并在每个Si-Si键中间插入O原子就成了SiO2的晶体结构模型.那么在SiO2晶体中,每个Si原子周围有 个O原子,每个O原子 个Si原子;每个Si原子周围有 个Si-O键,1mol SiO2中含有 mol Si-O键.

(1)在NaCl晶体中,在每个Na+离子的周围与它最接近的且距离相等的Na+离子共有
(2)在CsCl晶体中,每个Cs+离子周围与它最接近的且距离相等的Cs+离子共有
(3)在金刚石晶体中,每个C原子周围有
(4)如果将金刚石晶体结构模型中的C原子换成Si原子,并在每个Si-Si键中间插入O原子就成了SiO2的晶体结构模型.那么在SiO2晶体中,每个Si原子周围有
考点:晶胞的计算
专题:化学键与晶体结构
分析:(1)以顶点的钠离子为研究对象,与其最近的钠离子为面心的钠离子,则顶点钠离子被横平面、竖平面和侧平面共有,且每个平面与其距离最近的钠离子有4个;利用均摊法计算;
(2)Cs+离子位于顶点,被三条棱共有,每条棱有2个Cs+离子与它最接近的且距离相等,据此计算;每个顶点的Cs+离子被8个小立方体共有,Cl-离子位于立方体的体心,据此判断;
(3)根据图判断每个C原子可形成的C-C键数目;利用均摊法计算;
(4)根据金刚石中每个碳原子周围有四个碳原子;每个O原子形成两条共价键;金刚石中每个C原子可形成4条C-C键;金刚石中,碳碳键被两个碳原子共有,而每个Si可形成四条Si-O键.
(2)Cs+离子位于顶点,被三条棱共有,每条棱有2个Cs+离子与它最接近的且距离相等,据此计算;每个顶点的Cs+离子被8个小立方体共有,Cl-离子位于立方体的体心,据此判断;
(3)根据图判断每个C原子可形成的C-C键数目;利用均摊法计算;
(4)根据金刚石中每个碳原子周围有四个碳原子;每个O原子形成两条共价键;金刚石中每个C原子可形成4条C-C键;金刚石中,碳碳键被两个碳原子共有,而每个Si可形成四条Si-O键.
解答:
解:(1)以顶点的钠离子为研究对象,与其最近的钠离子为面心的钠离子,则顶点钠离子被横平面、竖平面和侧平面共有,且每个平面与其距离最近的钠离子有4个,则共有:3×4=12;根据图可知,Cl-离子位于棱心和体心,数目为:1+12×
=4,Na+离子位于顶点和面心,数目为:8×
+6×
=4,
故答案为:12;4;4;
(2)Cs+离子位于顶点,被三条棱共有,每条棱有2个Cs+离子与它最接近的且距离相等,则有2×3=6个;每个顶点的Cs+离子被8个小立方体共有,Cl-离子位于立方体的体心,则有8个Cl-离子与Cs+离子周围与它最接近的且距离相等,
故答案为:6;8;
(3)根据图判断每个C原子可形成的C-C键数目为4个;每条C-C键被两个C原子共有,每个碳原子可形成:4×
=2个C-C键,则1mol金刚石,含 C-C键2mol,
故答案为:4;2;
(4)由于金刚石晶体结构模型中的C原子换成Si原子,并在每个Si-Si键中间插入O原子就成了SiO2的晶体结构模型,根据金刚石中每个碳原子周围有四个碳原子,则每个Si原子周围有4个O原子;每个O原子与2个Si原子相连;金刚石中每个C原子可形成4条C-C键,则每个Si原子周围有4条Si-O键,故答案为:4;2;4;4.
| 1 |
| 4 |
| 1 |
| 8 |
| 1 |
| 2 |
故答案为:12;4;4;
(2)Cs+离子位于顶点,被三条棱共有,每条棱有2个Cs+离子与它最接近的且距离相等,则有2×3=6个;每个顶点的Cs+离子被8个小立方体共有,Cl-离子位于立方体的体心,则有8个Cl-离子与Cs+离子周围与它最接近的且距离相等,
故答案为:6;8;
(3)根据图判断每个C原子可形成的C-C键数目为4个;每条C-C键被两个C原子共有,每个碳原子可形成:4×
| 1 |
| 2 |
故答案为:4;2;
(4)由于金刚石晶体结构模型中的C原子换成Si原子,并在每个Si-Si键中间插入O原子就成了SiO2的晶体结构模型,根据金刚石中每个碳原子周围有四个碳原子,则每个Si原子周围有4个O原子;每个O原子与2个Si原子相连;金刚石中每个C原子可形成4条C-C键,则每个Si原子周围有4条Si-O键,故答案为:4;2;4;4.
点评:本题考查晶胞结构和配位数的计算,难度不大,要有一定的空间想象能力.

练习册系列答案
相关题目
下列关于有机化合物的说法正确的是( )
| A、乙酸和乙酸乙酯可用Na2CO3溶液加以区别 |
| B、戊烷(C5H12)有两种同分异构体 |
| C、将(NH4)2SO4、CuSO4溶液分别加入蛋白质溶液,都出现沉淀,表明二者均可使蛋白质变性 |
| D、糖类、油脂和蛋白质均可发生水解反应 |
2008年5月8日上午9时17分,北京奥运火炬祥云首次成功点亮在世界最高峰--珠峰,将奥运火送上珠峰,是一项艰巨和复杂的事情,对技术要求很高,充分体现了北京奥运会的“绿色奥运、科技奥运和人文奥运”的理念.北京奥运火炬的外壳主要采用高品质的铝合金材料制造,燃烧系统内装环保型燃料--丙烷.其下列对丙烷有关说法中不正确的是( )
| A、分子中碳原子不在一条直线上 |
| B、光照下能够发生取代反应 |
| C、比丁烷更易液化 |
| D、是石油分馏的一种产品 |
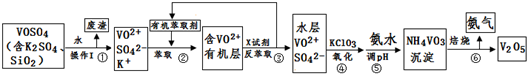
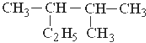 的名称是
的名称是