��Ŀ����
8��J��L��M��R��T��ԭ��������������Ķ���������Ԫ�أ�J��R�����ڱ��е����λ�����ұ���JԪ��������ϼ۵ľ���ֵ����ԭ��������������ȣ�M�ǵؿ��к������Ľ���Ԫ�أ�| J | ||||
| R |
 ��Ԫ��T���ڱ���λ�ڵڢ�A�壮
��Ԫ��T���ڱ���λ�ڵڢ�A�壮��2��J������ɵĻ����������4��ԭ�ӣ���ṹʽΪH-C��C-H��
��3��M��T�γɵĻ������ڳ�ʪ�Ŀ�����ð��ɫ��������Ӧ�Ļ�ѧ����ʽΪAlCl3+3H2O=Al��OH��3+3HCl����
��4��L�������̬�⻯���ˮ��Һ�Լ��ԣ�
�������ӹ�ҵ�У���ˮ��Һ������ʴ��H2O2 �����������������Ӧ�IJ��ﲻ��Ⱦ�������仯ѧ����ʽΪ2NH3•H2O+3H2O2=N2+8H2O��
���ɼ���������KOH ��Һ����ԭ��أ����������L�ĵ��ʣ����为����ӦʽΪ2NH3-6e-+6OH-�TN2+6H2O��
��5����J��R�γɵ�Һ̬������JR2 0.2mol��O2����ȫȼ�գ�����������̬�����298Kʱ�ų�����215kJ�� �÷�Ӧ���Ȼ�ѧ����ʽΪCS2��l��+3O2��g��=CO2��g��+2SO2��g����H=-1075KJ/mol��
���� J��L��M��R��T��ԭ��������������Ķ���������Ԫ�أ�M�ǵؿ��к������Ľ���Ԫ�أ���MΪAl����֪R��T���õ������ڣ���Ԫ��J��R�����ڱ��е����λ�ã���֪J���ڵڶ����ڣ���JԪ��������ϼ۵ľ���ֵ����ԭ��������������ȣ���J����������Ϊ4����JΪCԪ�أ���RΪSԪ�ء�TΪCl��L��ԭ����������̼����֮�䣬��LΪNԪ�أ�
��� �⣺J��L��M��R��T��ԭ��������������Ķ���������Ԫ�أ�M�ǵؿ��к������Ľ���Ԫ�أ���MΪAl����֪R��T���õ������ڣ���Ԫ��J��R�����ڱ��е����λ�ã���֪J���ڵڶ����ڣ���JԪ��������ϼ۵ľ���ֵ����ԭ��������������ȣ���J����������Ϊ4����JΪCԪ�أ���RΪSԪ�ء�TΪCl��L��ԭ����������̼����֮�䣬��LΪNԪ�أ�
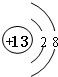
��1��MΪAl��������Ϊ13�������ӽṹʾ��ͼΪ ��TΪCl��λ�ڵڢ�A�壬�ʴ�Ϊ��
��TΪCl��λ�ڵڢ�A�壬�ʴ�Ϊ�� ����A��
����A��
��2��J������ɵĻ����������4��ԭ�ӣ�Ϊ��Ȳ���ṹʽΪH-C��C-H���ʴ�Ϊ��H-C��C-H��
��3��M��T�γɵĻ������ڳ�ʪ�Ŀ�����ð��ɫ����������ˮ�ⷴӦ���÷�Ӧ����ʽΪ��AlCl3+3H2O=Al��OH��3+3HCl����
�ʴ�Ϊ��AlCl3+3H2O=Al��OH��3+3HCl����
��4����LΪNԪ�أ�����⻯��Ϊ��������������ⷴӦ���ɵ�����ˮ����Ӧ����ʽΪ��2NH3•H2O+3H2O2=N2+8H2O��
�ʴ�Ϊ��2NH3•H2O+3H2O2=N2+8H2O��
�ڰ�����������KOH ��Һ����ԭ��أ���������������Ӧ��������������ӦΪ��2NH3-6e-+6OH-�TN2+6H2O��
�ʴ�Ϊ��2NH3-6e-+6OH-�TN2+6H2O��
��5��0.2mol CS2 ��O2����ȫȼ�գ�����������̬������Ϊ������̼�Ͷ�������298Kʱ�ų�����215kJ����1mol����̼��ȫȼ�������ȶ�������ų�������Ϊ215kJ��$\frac{1mol}{0.2mol}$=1075kJ�����Ȼ�ѧ��Ӧ����ʽΪ��CS2��l��+3O2��g��=CO2��g��+2SO2��g����H=-1075KJ/mol��
�ʴ�Ϊ��CS2��l��+3O2��g��=CO2��g��+2SO2��g����H=-1075KJ/mol��
���� ���⿼��ṹ����λ�ù�ϵӦ�ã��漰Ԫ�����ڱ������û�ѧ�������ˮ�⡢ԭ��ء��Ȼ�ѧ����ʽ��д�ȣ���Ŀ��Ϊ�ۺϣ���Ҫѧ���߱���ʵ��֪ʶ��������Ϣ������֪ʶ���������������������

��ش������й����⣺
��1������������ʾ��ijЩ�������ӵ�����������ȫ������pHΪ��
| ���� | Ca2+ | Fe3+ |
| ��ȫ����ʱ��pH | 13 | 3.7 |
�پƾ��� �������� ������ ������̨ �����ż� ��������
��2����KMnO4����Һ�ζ�C��Һʱ�������ķ�ӦΪ��5C2O42-+2MnO4-+16H+=10CO2��+2Mn2++8H2O��
�ֽ���ҺCϡ����500mL����ȡ���е�25.00mL��Һ���������ữ����0.1000mol•L-1��KMnO4����Һ�ζ����յ�ʱ����KMnO4��Һ10.00mL��
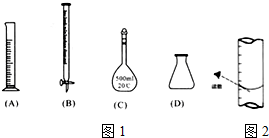
�˲�����������һ����Ҫ�õ�ͼ1����Щ��������д��ţ�BCD��
�ڴﵽ�ζ��յ�ʱ����Һ����ɫ�仯����ɫ��Ϊ��ɫ����������Һ����ɫ��
�۵ζ����յ㣬���ú���ͼ2��ȡKMnO4����Һ�Ŀ̶����ݣ���ⶨ�ĸ�Ԫ�غ�����ƫ�� ���ƫ�ߡ�����ƫ�͡�������Ӱ�족����
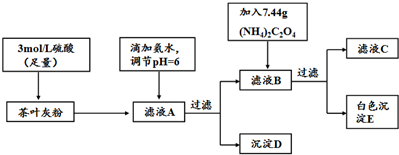
��3������ͨ��������ҺA����֤��Ʒ�Ʋ�Ҷ���Ƿ�����Ԫ�أ������Լ���ʵ��������KSCN��Һ����Һ�ʺ�ɫ��
| ���̿� | ��п�� |
| MnO2Լ70%��SiO2Լ20%��Al2O3Լ4%������Ϊˮ�� | ZnSԼ80%��FeS��CuS��SiO2��Լ7%������Ϊˮ�� |
��1�����̢�������Һ�к���MnSO4��ZnSO4��CuSO4��Fe2��SO4��3��Al2��SO4��3�ȣ������̢��б�������������FeS��CuS�֣�
��2�����̢��з�Ӧ�����ӷ���ʽΪZn+Fe3+=Fe2++Zn2+��Zn+Cu2+=Cu+Zn2+��
��3���������↑ʼ������pH�����
| �������� | Fe��OH��3 | Al��OH��3 | Fe��OH��2 |
| ��ʼ����pH | 1.5 | 3.3 | 7.6 |
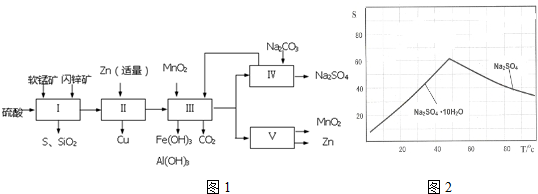
��4����ͼ2��Na2SO4��Na2SO4•10H2O���ܽ�ȣ�g/100gˮ�����ߣ���֪MnSO4��ZnSO4���ܽ�����¶ȵ����߶����������̢��õ�Na2SO4����IJ����ǣ��������MnCO3��ZnCO3�����Һ���½ᾧ�����ȹ��ˡ��Ҵ�ϴ�ӡ����Ҫ�����ȡ����˵�ԭ���Ƿ�ֹ�γ�Na2SO4•10H2O��
��5�����̢��������ǵ�⣬���ʱ���ö��Ե缫�����������ĵ缫��Ӧ�ɱ�ʾΪMn2+-2e-+2H2O=MnO2+4H+��
��6��ȡ1.95gп���뵽12.00mL 18.4mol/L��Ũ�����У���Ӧ��ֻ����һ�ֻ�ԭ�������ַ�Ӧ��С�ĵؽ���Һϡ�͵�1000mL��ȡ��15.00mL���Է�̪Ϊָʾ������0.25mol/L��NaOH��Һ�ζ����ᣬ����NaOH��Һ�����Ϊ21.70mL��
�ٷ�Ӧ����Һ�ж����������0.18 mol��
��ͨ������ȷ��Ũ���ᱻ��ԭ�IJ�����S��
| A�� | ��ϩ������ˮ���Ĵ���� | |
| B�� | �������������ʳƷ��Ư�� | |
| C�� | �������������ظ���������˾���Ƿ�Ƽ� | |
| D�� | ��ͭ��ͭп�Ͻ�������ͭ��ײ���ͭ�� |
| A�� | Ba2+ HCO3- K+ Cl- | B�� | CO32- OH- Na+ NO3- | ||
| C�� | OH- Na+ SO42- CO32- | D�� | Cu2+ Cl- Na+ NO3- |
| A�� | NH4Fe��SO4��2�������NaOH��Һ�У���NH4++Fe3++4OH-�TNH3•H2O+Fe��OH��3�� | |
| B�� | ����������Һ��ͨ������Ķ�������ClO-+SO2+H2O�THSO3-+HClO | |
| C�� | Ba��OH��2��Һ��ϡ���ᷴӦ��Ba2++OH-+H++SO42-�TBaSO4��+H2O | |
| D�� | �����ʯ��ˮ�м��������NaHCO3��Һ��Ca2++OH-+HCO3-�TCaCO3��+H2O |
 ��
��