题目内容
下列实验操作正确的是
A.过滤时为加快速度,可先将上层清液注入过滤器中,再将沉淀转移到过滤器中
B.蒸发时用玻璃棒搅拌,是为了使析出的固体重新溶解
C.蒸馏时需从冷凝管上口进水,下口出水
D.分液时,下层液体放完后,再从下口放出上层液体
A
【解析】
试题分析:A、过滤时为加快速度,因为上层清液含沉淀少过滤速率快,所以可先将上层清液注入过滤器中,再将沉淀转移到过滤器,A正确;B、在滤液蒸发时玻璃棒的作用是防止局部温度过高,使液滴飞溅,B错误;C、蒸馏时,为使冷凝水充满冷凝管,冷凝水应下进上出,C错误;D、分液时,下层液体从下口放出,再将上层液体从上口倒出,D错误。答案选A。
考点:考查物质的分离提纯。

下列叙述I和II均正确并有因果关系的是
选项 | 叙述I | 叙述II |
A | 实验室常用Al2(SO4)3溶液与氨水溶液制备Al(OH)3沉淀 | Al(OH)3不溶于碱 |
B | NaHCO3为强碱弱酸盐 | NaHCO3 溶液显碱性 |
C | SO2具有氧化性 | SO2可用品红溶液检验 |
D | Fe(OH)3胶体有丁达尔效应 | Fe(OH)3胶体可以用FeCl3浓溶液与NaOH溶液反应制得 |
(10分)(1)已知某反应的平衡常数表达式为:K= ,则它所对应反应的化学方程式是 。
,则它所对应反应的化学方程式是 。
(2)合成甲醇的主要反应是:2H2(g)+CO(g)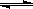 CH3OH(g) △H=-90.8 kJ·mol-1,t℃下此反应的平衡常数为160。此温度下,在密闭容器中开始只加入CO、H2,反应l0min后测得各组分的浓度如下:
CH3OH(g) △H=-90.8 kJ·mol-1,t℃下此反应的平衡常数为160。此温度下,在密闭容器中开始只加入CO、H2,反应l0min后测得各组分的浓度如下:
物质 | H2 | CO | CH3OH |
浓度(mol/L) | 0.2 | 0.1 | 0.4 |
(A)该时间段内反应速率v(H2)=
(B)比较此时正、逆反应速率的大小:v正 v逆(填“>”、“<”或“=”)
(C)反应达到平衡后,保持其它条件不变,若只把容器的体积缩小一半,平衡向
(填“逆向”、“正向”或“不”)移动,平衡常数K (填“增大”、“减小” 或“不变”)。
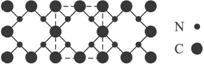
 g,一个12C的原子质量是b g,用NA是阿伏加德罗常数的值,下列叙述中不正确的是
g,一个12C的原子质量是b g,用NA是阿伏加德罗常数的值,下列叙述中不正确的是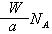 个原子
个原子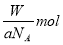 D.由已知信息可得:
D.由已知信息可得: mol-1
mol-1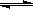 2C(g)+2D(g),在不同情况下测得反应速率如下,其中反应速率最快的是
2C(g)+2D(g),在不同情况下测得反应速率如下,其中反应速率最快的是