题目内容
有一种新燃料的电池,一极通入空气,另一极通入丁烷气体;电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-.下列对该燃料的说法不正确的是( )
| A、在熔融电解质中,O2-由负极移向正极 |
| B、电池的总反应是2C4H10+13O2→8CO2+10H2O |
| C、通入空气的一极是正极,电极反应为O2+4e-→2O2- |
| D、通入丁烷的一极是负极,电极反应为C4H10+13O2-→4CO2+5H2O+26e- |
考点:化学电源新型电池
专题:电化学专题
分析:在燃料电池中,负极发生氧化反应,电极反应式为C4H10-26e-+13O2-=4CO2+5H2O,正极发生还原反应,电极反应式为O2+4e-=2O2-,总反应式为2C4H10+13O2═8CO2+10H2O,在原电池中,阴离子向负极移动,阳离子向正极移动.
解答:
解:A、在原电池中,阴离子向负极移动,阳离子向正极移动,故A错误;
B、燃料电池的总反应与燃料燃烧的化学方程式相同,为2C4H10+13O2═8CO2+10H2O,故B正确;
C、通入空气的一极是正极,发生还原反应,电极反应为:O2+4e-=2O2-,故C正确;
D、丁烷具有还原性,在丁烷燃料电池中,负极发生氧化反应,电极反应式为C4H10-26e-+13O2-=4CO2+5H2O,故D正确.
故选A.
B、燃料电池的总反应与燃料燃烧的化学方程式相同,为2C4H10+13O2═8CO2+10H2O,故B正确;
C、通入空气的一极是正极,发生还原反应,电极反应为:O2+4e-=2O2-,故C正确;
D、丁烷具有还原性,在丁烷燃料电池中,负极发生氧化反应,电极反应式为C4H10-26e-+13O2-=4CO2+5H2O,故D正确.
故选A.
点评:本题考查化学电源新型电池,侧重于电极反应方程式的考查,题目难度中等,注意从正负极发生的变化结合电解质的特点书写电极反应式.

练习册系列答案
相关题目
下列实验方案设计中,可行的是( )
| A、焰色反应鉴别NaCl和NaNO2 |
| B、SiO2与H2O反应制取H2SiO3 |
| C、用氯气与烧碱溶液制备漂白粉 |
| D、用萃取的方法从碘的饱和水溶液中分离出碘 |
已知N2O4(g)?2NO2(g)△H>0,现将1mol N2O4充入一恒压密闭容器中,如图示意图正确且能说明反应达到平衡状态的是( )
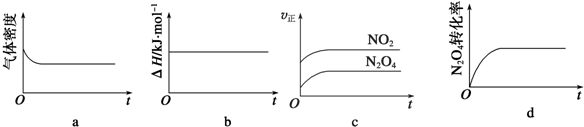

| A、ab | B、bc | C、ac | D、ad |
阿斯匹林的结构简式为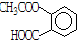 ,则1摩尔阿斯匹林和足量的NaOH溶液充分反应,消耗NaOH的物质的量为( )
,则1摩尔阿斯匹林和足量的NaOH溶液充分反应,消耗NaOH的物质的量为( )
 ,则1摩尔阿斯匹林和足量的NaOH溶液充分反应,消耗NaOH的物质的量为( )
,则1摩尔阿斯匹林和足量的NaOH溶液充分反应,消耗NaOH的物质的量为( )| A、1摩 | B、2摩 | C、3摩 | D、4摩 |
在一定条件下,测得2CO2?2CO+O2(反应从CO2开始)平衡体系的平均相对分子质量为M,在此条件下,CO2的分解率为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
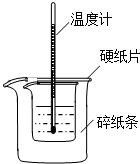 利用如图装置测定中和热的实验步骤如下:
利用如图装置测定中和热的实验步骤如下: