题目内容
如图表示A-I之间的转化关系.已知E无支链,E、G均可使溴的四氯化碳溶液褪色,有机物A、B和C在一定条件下可两两发生反应,1mol A、B、E、I均可与2mol NaHCO3反应.回答各问题:
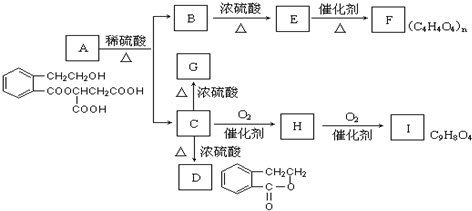
(1)A、B、C中所含相同官能团的名称为 ,F、I的结构简式分别为 , .
(2)E→F的反应类型为 ,C→G的反应类型为 .
(3)写出下列反应的化学方程式:B→E: ;C→H: .
(4)写出与C互为同分异构体且满足下列条件的物质的结构简式: .
①与氯化铁溶液发生显色反应
②苯环上有2个邻位取代基
③能发生银镜反应
④能发生水解反应.

(1)A、B、C中所含相同官能团的名称为
(2)E→F的反应类型为
(3)写出下列反应的化学方程式:B→E:
(4)写出与C互为同分异构体且满足下列条件的物质的结构简式:
①与氯化铁溶液发生显色反应
②苯环上有2个邻位取代基
③能发生银镜反应
④能发生水解反应.
考点:有机物的推断
专题:有机物的化学性质及推断
分析:A在稀硫酸、加热条件下发生水解反应生成 与
与 ,1molB与2molNaHCO3反应,故B为
,1molB与2molNaHCO3反应,故B为 ,C为
,C为 ,C氧化生成H,D氧化生成I,1molI可与2molNaHCO3反应,故H为
,C氧化生成H,D氧化生成I,1molI可与2molNaHCO3反应,故H为 ,I为
,I为 .C在浓硫酸、加热条件下生成G,G可使溴的四氯化碳溶液褪色,C发生消去反应生成G,则G为
.C在浓硫酸、加热条件下生成G,G可使溴的四氯化碳溶液褪色,C发生消去反应生成G,则G为 .C发生分子内酯化反应形成环酯D.B在浓硫酸作用下生成E,E可使溴的四氯化碳溶液褪色,1molE可与2molNaHCO3,应是B发生消去反应生成E,则E为HOOCCH=CHCOOH,E在催化剂条件下生成F,结合F的结构简式可知,E发生加聚反应生成F,故F为
.C发生分子内酯化反应形成环酯D.B在浓硫酸作用下生成E,E可使溴的四氯化碳溶液褪色,1molE可与2molNaHCO3,应是B发生消去反应生成E,则E为HOOCCH=CHCOOH,E在催化剂条件下生成F,结合F的结构简式可知,E发生加聚反应生成F,故F为 ,据此解答.
,据此解答.
 与
与 ,1molB与2molNaHCO3反应,故B为
,1molB与2molNaHCO3反应,故B为 ,C为
,C为 ,C氧化生成H,D氧化生成I,1molI可与2molNaHCO3反应,故H为
,C氧化生成H,D氧化生成I,1molI可与2molNaHCO3反应,故H为 ,I为
,I为 .C在浓硫酸、加热条件下生成G,G可使溴的四氯化碳溶液褪色,C发生消去反应生成G,则G为
.C在浓硫酸、加热条件下生成G,G可使溴的四氯化碳溶液褪色,C发生消去反应生成G,则G为 .C发生分子内酯化反应形成环酯D.B在浓硫酸作用下生成E,E可使溴的四氯化碳溶液褪色,1molE可与2molNaHCO3,应是B发生消去反应生成E,则E为HOOCCH=CHCOOH,E在催化剂条件下生成F,结合F的结构简式可知,E发生加聚反应生成F,故F为
.C发生分子内酯化反应形成环酯D.B在浓硫酸作用下生成E,E可使溴的四氯化碳溶液褪色,1molE可与2molNaHCO3,应是B发生消去反应生成E,则E为HOOCCH=CHCOOH,E在催化剂条件下生成F,结合F的结构简式可知,E发生加聚反应生成F,故F为 ,据此解答.
,据此解答.解答:
解:A在稀硫酸、加热条件下发生水解反应生成 与
与 ,1molB与2molNaHCO3反应,故B为
,1molB与2molNaHCO3反应,故B为 ,C为
,C为 ,C氧化生成H,D氧化生成I,1molI可与2molNaHCO3反应,故H为
,C氧化生成H,D氧化生成I,1molI可与2molNaHCO3反应,故H为 ,I为
,I为 .C在浓硫酸、加热条件下生成G,G可使溴的四氯化碳溶液褪色,C发生消去反应生成G,则G为
.C在浓硫酸、加热条件下生成G,G可使溴的四氯化碳溶液褪色,C发生消去反应生成G,则G为 .C发生分子内酯化反应形成环酯D.B在浓硫酸作用下生成E,E可使溴的四氯化碳溶液褪色,1molE可与2molNaHCO3,应是B发生消去反应生成E,则E为HOOCCH=CHCOOH,E在催化剂条件下生成F,结合F的结构简式可知,E发生加聚反应生成F,故F为
.C发生分子内酯化反应形成环酯D.B在浓硫酸作用下生成E,E可使溴的四氯化碳溶液褪色,1molE可与2molNaHCO3,应是B发生消去反应生成E,则E为HOOCCH=CHCOOH,E在催化剂条件下生成F,结合F的结构简式可知,E发生加聚反应生成F,故F为 ,
,
(1)B为 ,C为
,C为 ,结合A的结构简式,可知A、B、C中所含相同官能团的名称为:羧基、醇羟基.由上述分析可知,F为
,结合A的结构简式,可知A、B、C中所含相同官能团的名称为:羧基、醇羟基.由上述分析可知,F为 ,I为
,I为 ,
,
故答案为:羧基、醇羟基; ;
; ;
;
(2)E→F是HOOCCH=CHCOOH发生加聚反应生成 ,C→G是
,C→G是 在浓硫酸、加热条件下发生消去反应生成
在浓硫酸、加热条件下发生消去反应生成 ,故答案为:加聚反应;消去反应;
,故答案为:加聚反应;消去反应;
(3)B→E的化学方程式为:
HOOCCH=CHCOOH+H2O,
C→H的化学方程式为:2 +O2
+O2
2 +2H2O,
+2H2O,
故答案为:
HOOCCH=CHCOOH+H2O;2 +O2
+O2
2 +2H2O;
+2H2O;
(4)与C( )互为同分异构体且满足下列条件:
)互为同分异构体且满足下列条件:
与氯化铁溶液发生显色反应,含有酚羟基,能发生银镜反应且能发生水解反应,含有-OOCH,苯环上有2个邻位取代基,符合条件的同分异构体为: ,
,
故答案为: .
.
 与
与 ,1molB与2molNaHCO3反应,故B为
,1molB与2molNaHCO3反应,故B为 ,C为
,C为 ,C氧化生成H,D氧化生成I,1molI可与2molNaHCO3反应,故H为
,C氧化生成H,D氧化生成I,1molI可与2molNaHCO3反应,故H为 ,I为
,I为 .C在浓硫酸、加热条件下生成G,G可使溴的四氯化碳溶液褪色,C发生消去反应生成G,则G为
.C在浓硫酸、加热条件下生成G,G可使溴的四氯化碳溶液褪色,C发生消去反应生成G,则G为 .C发生分子内酯化反应形成环酯D.B在浓硫酸作用下生成E,E可使溴的四氯化碳溶液褪色,1molE可与2molNaHCO3,应是B发生消去反应生成E,则E为HOOCCH=CHCOOH,E在催化剂条件下生成F,结合F的结构简式可知,E发生加聚反应生成F,故F为
.C发生分子内酯化反应形成环酯D.B在浓硫酸作用下生成E,E可使溴的四氯化碳溶液褪色,1molE可与2molNaHCO3,应是B发生消去反应生成E,则E为HOOCCH=CHCOOH,E在催化剂条件下生成F,结合F的结构简式可知,E发生加聚反应生成F,故F为 ,
,(1)B为
 ,C为
,C为 ,结合A的结构简式,可知A、B、C中所含相同官能团的名称为:羧基、醇羟基.由上述分析可知,F为
,结合A的结构简式,可知A、B、C中所含相同官能团的名称为:羧基、醇羟基.由上述分析可知,F为 ,I为
,I为 ,
,故答案为:羧基、醇羟基;
 ;
; ;
;(2)E→F是HOOCCH=CHCOOH发生加聚反应生成
 ,C→G是
,C→G是 在浓硫酸、加热条件下发生消去反应生成
在浓硫酸、加热条件下发生消去反应生成 ,故答案为:加聚反应;消去反应;
,故答案为:加聚反应;消去反应;(3)B→E的化学方程式为:

| 浓硫酸 |
| △ |
C→H的化学方程式为:2
 +O2
+O2| 催化剂 |
| △ |
 +2H2O,
+2H2O,故答案为:

| 浓硫酸 |
| △ |
 +O2
+O2| 催化剂 |
| △ |
 +2H2O;
+2H2O;(4)与C(
 )互为同分异构体且满足下列条件:
)互为同分异构体且满足下列条件:与氯化铁溶液发生显色反应,含有酚羟基,能发生银镜反应且能发生水解反应,含有-OOCH,苯环上有2个邻位取代基,符合条件的同分异构体为:
 ,
,故答案为:
 .
.
点评:本题考查有机物推断,涉及官能团、限制条件同分异构体的书写、有机反应类型、有机方程式书写等,根据官能团的性质结合A的结构与题目信息确定B、C的结构是解本题的关键,需要学生熟练掌握官能团的性质与转化,难度中等.

练习册系列答案
相关题目
已知:H2C2O4、KMnO4、H2SO4混合发生反应:5H2C2O4+2MnO4-+6H+=2Mn2++10CO2↑+8H2O.某同学根据上述原理和溶液褪色时间,设计实验测定反应速率,实验记录如下表(各实验均在室温下进行):下列结论正确的是( )
| 实验编号 | 烧杯中所加的试剂及其用量(mL) | 加入少 量固体 | 溶液褪色 时间(s) | |||
| 0.6mol/L H2C2O4溶液 | H2O | 0.2mol/L KMnO4溶液 | 3mol/L 稀硫酸 | |||
| 1 | 30.0 | 20.0 | 30.0 | 20.0 | 无 | 1.8 |
| 2 | 15.0 | 15.0 | 10.0 | 无 | 3.6 | |
| 3 | 30.0 | 20.0 | 30.0 | 20.0 | K2SO4 | 1.8 |
| 4 | 30.0 | 20.0 | 30.0 | 20.0 | MnSO4 | 0.6 |
| A、实验3、4说明K+对该反应有催化作用 |
| B、实验2中x=10 |
| C、实验1、2说明反应速率只与KMnO4浓度有关 |
| D、实验1、4可推出实验1中反应速率变化:起初较小,后明显变大,又逐渐变小 |
 某研究性学习小组对铝热反应实验展开研究.现行高中化学教材中对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”、“纸漏斗的下部被烧穿,有熔融物落入沙中”.查阅《化学手册》知,Al、Al2O3、Fe、Fe2O3熔点、沸点数据如下:
某研究性学习小组对铝热反应实验展开研究.现行高中化学教材中对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”、“纸漏斗的下部被烧穿,有熔融物落入沙中”.查阅《化学手册》知,Al、Al2O3、Fe、Fe2O3熔点、沸点数据如下: