题目内容
6.在一固定体积的密闭容器中,充入2mol CO2和1mol H2发生如下化学反应:CO2(g)+H2(g)?CO(g)+H2O(g),其化学平衡常数与温度(T)的关系如下表:| T/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应的化学平衡常数表达式为K=$\frac{c(CO)•c({H}_{2}O)}{c(C{O}_{2})•c({H}_{2})}$.
(2)若反应在830℃下达到平衡,则CO2气体的转化率为33.3%.
(3)若绝热时(容器内外没有热量交换),平衡发生移动的结果是使容器内CO2的浓度增大,则容器内气体温度升高(填“升高”、“降低”或“不能确定”).
(4)能判断该反应是否达到化学平衡状态的依据是AD(填字母序号).
A.H2的浓度保持不变
B.容器内的总压强不随时间而变化
C.单位时间内生成n mol CO的同时,生成n mol的H2O
D.υ(正、CO)=υ(逆、CO2)
分析 (1)平衡常数是指:一定温度下,可逆反应到达平衡时,生成物浓度系数次幂乘积与反应物浓度系数次幂乘积的比;
(2)令平衡时参加反应的CO2的物质的量为ymol,则:
CO2(g)+H2(g)?CO(g)+H2O(g)
开始(mol):2 1 0 0
变化(mol):y y y y
平衡(mol):2-y 1-y y y
再根据平衡常数K=1列方程计算解答;
(3)由表中数据可知,温度升高平衡常数增大,说明平衡向正反应方向移动,则正反应为吸热反应.若绝热时(容器内外没有热量交换),平衡发生移动的结果是使容器内CO的浓度增大,则平衡正向移动;
(4)可逆反应到达平衡时,同种物质的正逆速率相等,各组分的浓度、含量保持不变,由此衍生的其它一些量不变,判断平衡的物理量应随反应进行发生变化,该物理量由变化到不变化说明到达平衡
解答 解:(1)CO2(g)+H2(g)?CO(g)+H2O(g)平衡常数表达式K=$\frac{c(CO)•c({H}_{2}O)}{c(C{O}_{2})•c({H}_{2})}$;
故答案为:$\frac{c(CO)•c({H}_{2}O)}{c(C{O}_{2})•c({H}_{2})}$;
(2)令平衡时参加反应的CO2的物质的量为ymol,则:
CO2(g)+H2(g)?CO(g)+H2O(g)
开始(mol):2 1 0 0
变化(mol):y y y y
平衡(mol):2-y 1-y y y
则$\frac{y×y}{(2-y)×(1-y)}$=1,解得y=$\frac{2}{3}$,故CO2气体的转化率为$\frac{\frac{2}{3}mol}{2mol}$×100%=33.3%,
故答案为:33.3%;
(3)由表中数据可知,温度升高,平衡常数增大,说明平衡向正反应方向移动,则正反应为吸热反应.若绝热时(容器内外没有热量交换),平衡发生移动的结果是使容器内CO2的浓度增大,则平衡逆向移动,放出热量,故容器内气体温度升高;
故答案为:升高;
(4)A.混合气体中c(CO)不变,说明到达平衡,故A正确;
B.由于反应前后气体体积不变,容器内压强始终不变,不能说明到达平衡,故B错误;
C.单位时间内生成n mol CO的同时,生成n mol的H2O,都体现正反应的方向,未体现正与逆的关系,不能说明到达平衡,故C错误;
D.υ(正、CO)=υ(逆、CO2),说明CO的生成速率与消耗速率相等,说明到达平衡,故D正确;
故选:AD.
点评 本题考查化学平衡常数的应用、化学平衡移动,平衡状态判断等,难度中等,掌握化学平衡常数的书写与应用,比较容易.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 看外观 | B. | 加热 | ||
| C. | 分析粒子直径大于10-7cm | D. | 发生丁达尔现象 |
| A. | FeCl2溶液 | B. | 溴水 | C. | NaOH溶液 | D. | 水 |
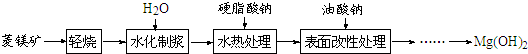
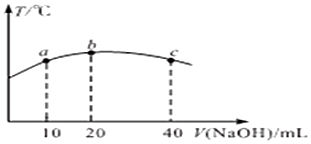
(1)从图1和图2可以得出的结论为随着水化时间延长,MgO的量不断减少,Mg(OH)2的量不断增加、温度升高,水化反应速率加快.

(2)水化反应MgO+H2O═Mg(OH)2能自发进行的原因是△H<0.
(3)结合元素周期律和下表可知,金属氢氧化物受热分解的规律有金属离子半径越大,氢氧化物越难分解(或金属性越强,氢氧化物越难分解等).(写一条即可)
部分主族元素的金属氢氧化物热分解温度/℃
| LiOH | NaOH | KOH | Al(OH)3 | Mg(OH)2 | Ca(OH)2 | Ba(OH)2 |
| 924 | 不分解 | 不分解 | 140 | 258 | 390 | 700 |
①Mg(OH)2起阻燃作用的主要原因是Mg(OH)2分解时吸热,使环境温度下降;同时生成的耐高温、稳定性好的MgO覆盖在可燃物表面,阻燃效果更佳.
②与常用卤系(如四溴乙烷)和有机磷系(磷酸三苯酯)阻燃剂相比,Mg(OH)2阻燃剂的优点是无烟、无毒、腐蚀性小.
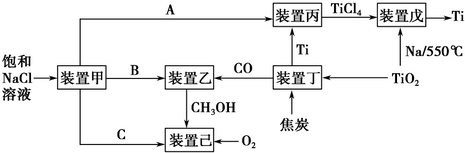
请回答下列问题:
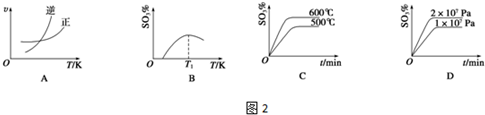
(1)装置甲为电解池(惰性电极),根据图示转化关系可知:A为Cl2(填化学式),阴极反应式为2H++2e-=H2 ↑.
(2)装置丙的反应物为Ti,而装置戊的生成物为Ti,这两个装置在该联合生产中并不矛盾,原因是进入装置丙的Ti含有的杂质较多,从装置戊中出来的Ti较为纯净装置戊进行反应时需要的环境为C(填字母序号).
A.HCl气体氛围中 B.空气氛围中 C.氩气氛围中 D.水中
(3)装置乙中发生的是工业合成甲醇的反应:CO(g)+2H2(g)=CH3OH(g)△H<0.
①该反应在不同温度下的化学平衡常数(K)如下表:
| 温度/℃ | 250 | 350 |
| K | 2.041 | x |
A.0 B.0.012 C.32.081 D.100
②若装置乙为容积固定的密闭容器,不同时间段各物质的浓度如下表:
| c(CO)/mol•L-1 | c(H2)/mol•L-1 | c(CH3OH)/mol•L-1 | |
| 0min | 0.8mol•L-1 | 1.6mol•L-1 | 0 |
| 2min | 0.6mol•L-1 | y | 0.2mol•L-1 |
| 4min | 0.3mol•L-1 | 0.6mol•L-1 | 0.5mol•L-1 |
| 6min | 0.3mol•L-1 | 0.6mol•L-1 | 0.5mol•L-1 |
A.使用催化剂 B.降低温度 C.增加H2的浓度.
| A. | 将一种气体通入品红溶液,溶液褪色,说明该气体一定是二氧化硫 | |
| B. | K+、NH4+、SO42-、CO32-离子组在加入铝粉能放出大量H2的溶液中一能能大量共存 | |
| C. | FeBr2溶液中通入过量Cl2时的离子方程式为:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- | |
| D. | 在纯碱溶液中逐滴加入稀盐酸时,开始没有气泡产生 |