题目内容
下列陈述正确的是( )
| A、氢氧化铁胶体稳定存在的主要原因是氢氧化铁胶体带正电荷 |
| B、向BaCl2溶液中通入SO2气体会产生白色沉淀 |
| C、CaCO3(s)═CaO(s)+CO2(g)室温下不能自发进行,说明该反应的△H<0 |
| D、CuSO4?5H2O是一种纯净物 |
考点:胶体的重要性质,混合物和纯净物,反应热和焓变
专题:
分析:A.胶体整体上不带电,氢氧化铁胶粒带正电荷;
B.BaCl2溶液与通入SO2气体不反应;
C.根据反应可知△S>0,室温下不能自发进行,说明该反应的△H>0,故C错误;
D.五水硫酸铜是一种结晶水合物,是一种纯净物.
B.BaCl2溶液与通入SO2气体不反应;
C.根据反应可知△S>0,室温下不能自发进行,说明该反应的△H>0,故C错误;
D.五水硫酸铜是一种结晶水合物,是一种纯净物.
解答:
解:A.胶体整体上不带电,氢氧化铁胶体稳定存在的主要原因是氢氧化铁胶粒带正电荷,故A错误;
B.向BaCl2溶液中通入SO2气体不会产生白色沉淀,故B错误;
C.CaCO3(s)═CaO(s)+CO2(g)气体的量增大,△S>0,因为室温下不能自发进行,说明该反应的△H>0,故C错误;
D.五水硫酸铜是一种结晶水合物,是一种纯净物,故D正确;
故选D.
B.向BaCl2溶液中通入SO2气体不会产生白色沉淀,故B错误;
C.CaCO3(s)═CaO(s)+CO2(g)气体的量增大,△S>0,因为室温下不能自发进行,说明该反应的△H>0,故C错误;
D.五水硫酸铜是一种结晶水合物,是一种纯净物,故D正确;
故选D.
点评:本题考查了、胶体的性质、混合物与纯净物、化学反应的方向等问题,难度不大.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
相关题目
对于Cl2+SO2+2H2O═H2SO4+2HCl反应,下列说法正确的是( )
①Cl2是氧化剂 ②SO2被氧化 ③Cl2被氧化 ④Cl2发生还原反应 ⑤SO2具有还原性 ⑥Cl2具有氧化性.
①Cl2是氧化剂 ②SO2被氧化 ③Cl2被氧化 ④Cl2发生还原反应 ⑤SO2具有还原性 ⑥Cl2具有氧化性.
| A、只有①②⑥ |
| B、只有②③④ |
| C、只有②④⑤⑥ |
| D、只有①②④⑤⑥ |
某有机物的结构简式如图所示,下列说法错误的是( )
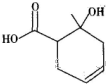

| A、该物质能和氯化铁溶液发生显色反应 |
| B、该物质含有两种含氧官能团 |
| C、该物质可使溴的四氯化碳溶液褪色 |
| D、该物质既可以发生取代反应又可以发生加成反应 |
2.8g铁与0.1L稀硝酸混合后充分反应,产生气体为NO,反应后Fe、硝酸均无剩余.向反应后的溶液中加入0.1L 0.2mol/LKI溶液,恰好将溶液中的Fe3+全部还原.则原溶液硝酸的物质的量浓度为( )
| A、1.2mol/l |
| B、1.6mol/l |
| C、2mol/l |
| D、1.3mol/l |
下列变化过程,属于放热反应的是( )
①液态水变成水蒸气
②酸碱中和反应
③浓H2SO4稀释
④固体NaOH溶于水
⑤H2在Cl2中燃烧
⑥铝与Fe2O3高温下反应.
①液态水变成水蒸气
②酸碱中和反应
③浓H2SO4稀释
④固体NaOH溶于水
⑤H2在Cl2中燃烧
⑥铝与Fe2O3高温下反应.
| A、①③④⑤ | B、②③④ |
| C、②③④⑤ | D、②⑤⑥ |
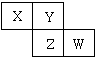 如图是元素周期表的一部分.X、Y、Z、W均为短周期元素,若W原子最外电子层电子数是其内层电子数的
如图是元素周期表的一部分.X、Y、Z、W均为短周期元素,若W原子最外电子层电子数是其内层电子数的| 7 |
| 10 |
| A、X元素的氢化物水溶液呈碱性 |
| B、气态氢化物的稳定性:Y>Z |
| C、最高氧化物对应水化物的酸性:W>Z |
| D、阴离子半径从大到小排列的顺序:Y>Z>W |
 CCTV-1《焦点访谈》栏目中曾报道“铊中毒事件”,铊再次成为公众关注的焦点.铊的相关信息如图,其中“6s26p1”表示铊原子有6个电子层,最外层有3个电子.下列有关卡片信息解读不正确的是( )
CCTV-1《焦点访谈》栏目中曾报道“铊中毒事件”,铊再次成为公众关注的焦点.铊的相关信息如图,其中“6s26p1”表示铊原子有6个电子层,最外层有3个电子.下列有关卡片信息解读不正确的是( )| A、铊的元素符号为Tl |
| B、铊原子的中子数为204 |
| C、铊位于第六周期ⅢA族 |
| D、铊的金属性比铝的金属性强 |
下列实验操作不正确的是( )
| A、NaCl溶液蒸发结晶时,蒸发皿中有晶体析出并剩余少量液体时即停止加热 |
| B、除去Fe(OH)3胶体中混有的Cl-离子,可用渗析的方法 |
| C、蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 |
| D、用四氯化碳萃取碘时,碘的四氯化碳溶液从分液漏斗上口倒出 |