题目内容
硫酸工业尾气中二氧化硫含量超过0.05%(体积分数)时需经处理后才能排放。某校兴趣小组欲测定硫酸工业尾气中二氧化硫含量,采用以下方案:
甲方案:如图所示,图中气体流量计B用于准确测量通过尾气的体积。将尾气通入一定体积已知浓度的碘水中测定二氧化硫的含量。当洗气瓶C中溶液蓝色消失时,立即关闭活塞A。

(1)洗气瓶C中导管末端连接一个多孔球泡D,可以提高实验准确度,其理由是
。
(2)洗气瓶C中的溶液可以用其他试剂替代,请你举出一种: 。
(3)洗气瓶C溶液蓝色消失后,没有及时关闭活塞A,测得的SO2含量 (填“偏高”“偏低”或“无影响”)。
乙方案:实验步骤如以下流程图所示:
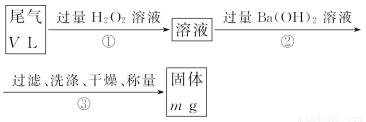
(4)写出步骤②中反应的化学方程式 。
(5)步骤③中洗涤沉淀的方法是 。
(6)通过的尾气体积为VL(已换算成标准状况)时,该尾气中二氧化硫含量(体积分数)为 (用含有V、m的代数式表示)。
丙方案:将乙方案中步骤①省略,直接将尾气通入过量Ba(OH)2溶液,其余步骤与乙方案相同。
(7)你认为丙方案是否合理,说明理由:
。
(1)增大SO2与碘水的接触面积,使SO2和碘水充分反应 (2)酸性高锰酸钾溶液或溴水
(3)偏低 (4)H2SO4+Ba(OH)2====BaSO4↓+2H2O
(5)向漏斗里注入蒸馏水,使水面没过沉淀物,待水流尽后,重复操作2~3次
(6)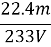 (7)不合理,BaSO3被部分氧化为BaSO4
(7)不合理,BaSO3被部分氧化为BaSO4
【解析】
试题分析:(1)甲方案利用的原理为SO2+I2+2H2O====H2SO4+2HI,最后测定剩余气体的体积,进而测定尾气中二氧化硫的含量,洗气瓶C中导管末端连接一个多孔球泡D,可以增大SO2与碘水的接触面积,使SO2和碘水充分反应;(2)洗气瓶C中的溶液还可以用酸性高锰酸钾溶液、溴水等代替;(3)洗气瓶C中溶液蓝色消失后,没有及时关闭活塞A,则通入尾气的体积增大,因此SO2含量偏低;(4)乙方案利用的原理为SO2+H2O2====H2SO4,H2SO4+Ba(OH)2====BaSO4↓+2H2O,最后根据沉淀硫酸钡的质量计算尾气中二氧化硫的质量,进而计算尾气中二氧化硫的含量。步骤②中反应的化学方程式为H2SO4+Ba(OH)2====BaSO4↓+2H2O;(5)洗涤沉淀的方法是:向漏斗里注入蒸馏水,使水面没过沉淀物,待水流尽后,重复操作2~3次;(6)mg是硫酸钡的质量,硫酸钡的物质的量为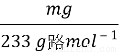 =
=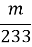 mol,根据硫元素守恒可知二氧化硫的体积为
mol,根据硫元素守恒可知二氧化硫的体积为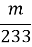 mol×22.4 L·mol-1=
mol×22.4 L·mol-1=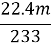 L,故尾气中二氧化硫的体积分数为
L,故尾气中二氧化硫的体积分数为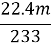 L÷VL=
L÷VL=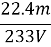 ;(7)丙方案将乙方案中步骤①省略,直接将尾气通入过量Ba(OH)2溶液,生成的BaSO3会被部分氧化为BaSO4,导致测定的亚硫酸钡的质量偏大,测定二氧化硫的体积偏大,体积分数偏大,故不合理。
;(7)丙方案将乙方案中步骤①省略,直接将尾气通入过量Ba(OH)2溶液,生成的BaSO3会被部分氧化为BaSO4,导致测定的亚硫酸钡的质量偏大,测定二氧化硫的体积偏大,体积分数偏大,故不合理。
考点:二氧化硫的性质和作用

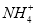 中,NH3发生氧化反应
中,NH3发生氧化反应