题目内容
14.下列说法正确的是( )| A. | 蔗糖加稀硫酸水解后,加入新制氢氧化铜溶液,煮沸,可以检验产物是否含有葡萄糖 | |
| B. | 钠可保存在煤油中,而钠可与乙醇发生反应,可说明乙醇分子含有羟基的氢原子 | |
| C. | 可用溴水鉴别乙醇、己烷、硝基苯、乙酸 | |
| D. | 乙酸乙酯和乙醇可用分液的方式分离 |
分析 A.水解生成葡萄糖和果糖,检验葡萄糖应在碱性条件下;
B.钠的密度比煤油的大,且不反应;钠与乙醇反应生成氢气,-OH上O-H键断裂;
C.乙醇、乙酸均与溴水互溶,不分层;
D.乙酸乙酯和乙醇不分层.
解答 解:A.水解生成葡萄糖和果糖,检验葡萄糖应在碱性条件下,则水解后先加碱至碱性再加入新制氢氧化铜溶液,煮沸,检验产物是否含有葡萄糖,故A错误;
B.钠的密度比煤油的大,且不反应,钠可保存在煤油中;钠与乙醇反应生成氢气,-OH上O-H键断裂,则可说明乙醇分子含有羟基的氢原子,故B正确;
C.乙醇、乙酸均与溴水互溶,不分层,现象相同不能鉴别,故C错误;
D.乙酸乙酯和乙醇不分层,不能分液分离,故D错误;
故选B.
点评 本题考查有机物的结构与性质,为高考常见题型,把握有机物的组成、结构、性质及官能团为解答的关键,侧重分析与应用能力的考查,注意有机物的鉴别方法,题目难度不大.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案
相关题目
5.将下列物质按酸、碱、盐分类顺序排列正确的是( )
| A. | 硝酸 小苏打 硫酸钾 | B. | 硅酸 熟石灰 生石灰 | ||
| C. | 硫酸 烧碱 硫酸铝 | D. | 盐酸 纯碱 食盐 |
9.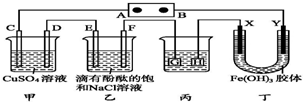 如图装置所示,C、D、E、F、X、Y都是惰性电极,A、B为外接直流电源的两极.将直流电源接通后,F极附近呈红色.下列叙述正确的是( )
如图装置所示,C、D、E、F、X、Y都是惰性电极,A、B为外接直流电源的两极.将直流电源接通后,F极附近呈红色.下列叙述正确的是( )
 如图装置所示,C、D、E、F、X、Y都是惰性电极,A、B为外接直流电源的两极.将直流电源接通后,F极附近呈红色.下列叙述正确的是( )
如图装置所示,C、D、E、F、X、Y都是惰性电极,A、B为外接直流电源的两极.将直流电源接通后,F极附近呈红色.下列叙述正确的是( )| A. | A是电源的负极 | |
| B. | 若C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为2:1:1:1 | |
| C. | 用丙装置给铜件镀银,则G应是铜件 | |
| D. | 丁中Y极附近的颜色逐渐变深,表明Fe(OH)3胶体胶粒带正电荷 |
19.下列装置进行有关实验不能达到预期目的是( )

| A. | 若图Ⅰ所示实验中反应速率为①>②,则一定说明Fe3+比Cu2+对H2O2分解催化效果好 | |
| B. | 用图2装置可测定过氧化氢分解反应产生气体体积(液体体积忽略) | |
| C. | 用图3装置制备金属锰 | |
| D. | 用图4装置可验证化学能转化为电能 |
6.2005年11月18日国际著名血液学杂志《BLOOD》刊载了一条令人振奋的科研成果,中国科学家找到白血病的致病元凶--蛋白质Shp-2.下列关于蛋白质Shp-2说法正确的是( )
| A. | 它是高分子化合物 | |
| B. | 天然蛋白质仅由碳、氢、氧、氮四种元素组成 | |
| C. | 在一定条件下能水解最终生成多肽 | |
| D. | 氨基酸和蛋白质Shp-2都只能与碱反应 |
14.25℃、101kPa下,煤炭、氢气、天然气和甲醇(CH3OH)等几种燃料的热值(指一定条件下单位质量的物质完全燃烧所放出的热量)依次是33kJ•g-1、143kJ•g-1、56kJ•g-1、23kJ•g-1,则下列热化学方程式正确的是( )
| A. | C(s)+$\frac{1}{2}$O2(g)=CO(g)△H=-396 kJ•mol-1 | |
| B. | CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-896 kJ•mol-1 | |
| C. | 2H2(g)+O2(g)=2H2O(l)△H=-286 kJ•mol-1 | |
| D. | CH3OH(l)+$\frac{3}{2}$O2(g)=CO2(g)+2H2O(l)△H=+736kJ•mol-1 |
 一定温度下,在一容积不变的容器中,发生化学反应aA(g)+bB(g)═cC(g),采用不同比例的A,B作为起始物,测量反应达平衡时A和B的转化率,得到如图图象:
一定温度下,在一容积不变的容器中,发生化学反应aA(g)+bB(g)═cC(g),采用不同比例的A,B作为起始物,测量反应达平衡时A和B的转化率,得到如图图象: