题目内容
19.用NA表示阿伏加德罗常数的值,下列叙述正确的是( )| A. | 含有NA个氢原子的氢气在标准状况下的体积约为22.4L | |
| B. | 25℃,1.01×105Pa,64gSO2中含有的原子数为3NA | |
| C. | 在常温常压下,11.2LCl2含有的分子数为0.5NA | |
| D. | 标准状况下,11.2LH2O含有的分子数为0.5NA |
分析 A、根据V=nVm=$\frac{N}{{N}_{A}}$Vm来计算;
B、根据m=nM=$\frac{N}{{N}_{A}}$M来计算;
C、根据N=nNA=$\frac{V}{Vm}$NA来计算;
D、标准状况下,水不是气体,11.2LH2O不一定是0.5mol.
解答 解:A、含有NA个氢原子的氢气在标准状况下的体积约为22.4L/mol×$\frac{{N}_{A}}{{N}_{A}}$×$\frac{1}{2}$mol=11.2L,故A错误;
B、25℃,1.01×105Pa,64gSO2中含有的原子数为$\frac{64g}{64g/mol}×3$NA=3NA,故B正确;
C、在常温常压下,11.2LCl2的物质的量无法计算,体积无法计算,故C错误;
D、标准状况下,水不是气体,11.2LH2O不一定是0.5mol,分子数无法计算,故D错误.
故选B.
点评 本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,阿伏加德罗常数是高考的“热点,要准确解答好这类题目,一是要掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系;二是要准确弄清分子、原子、原子核内质子中子及核外电子的构成关系.

练习册系列答案
相关题目
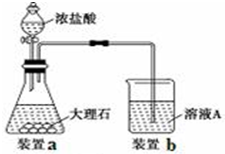
15.在足量的稀氯化亚铁溶液中,加入1~2滴液溴,振荡后溶液变为黄色.
(1)甲同学认为这不是发生化学反应所致,使溶液变黄色的物质是:Br2;
乙同学认为这是发生化学反应所致,使溶液变黄色的微粒是Fe3+,写出反应离子方程式2Fe2++Br2=Fe3++2Br+
(2)实验证明乙同学推断是正确的,请用两种方法加以验证,写出选用的试剂编号及实验中观察到的现象.
A.酸性高锰酸钾溶液 B.氢氧化钠溶液 C.四氯化碳 D.硫氰化钾溶液
写出任意一种检验方法所涉及的离子方程式Fe3++3SCN-=Fe(SCN)3.
(1)甲同学认为这不是发生化学反应所致,使溶液变黄色的物质是:Br2;
乙同学认为这是发生化学反应所致,使溶液变黄色的微粒是Fe3+,写出反应离子方程式2Fe2++Br2=Fe3++2Br+
(2)实验证明乙同学推断是正确的,请用两种方法加以验证,写出选用的试剂编号及实验中观察到的现象.
A.酸性高锰酸钾溶液 B.氢氧化钠溶液 C.四氯化碳 D.硫氰化钾溶液
| 选用试剂 | 实验现象 | |
| 第一种方法 | C | 有机层(下层)无色 |
| 第二种方法 | D | 溶液呈血红色 |
4.“善待地球-科学发展,构建和谐”是“世界地球日”的主题.你认为下列行为不符合这一主题的是( )
| A. | 控制含磷洗涤剂的生产和使用,防止水体富营养化,保护水资源 | |
| B. | 开发太阳能、水能、风能、可燃冰等新能源,减少使用煤、石油等化石燃料 | |
| C. | 研究采煤、采油新技术,尽量提高产量以满足工业生产的快速发展 | |
| D. | 实现资源的“3R”利用,即:减少资源消耗(Reduce)、增加资源的重复使用(Reuse)、资源的循环再生(Recycle) |
8.宇宙星球中蕴藏着大量人类可利用的资源.月球土壤中吸附着数万吨可作为核聚变材料的23He.下列有关23He的说法正确的是( )
| A. | 质子数为1 | B. | 电子数为3 | C. | 中数为2 | D. | 质量数为3 |


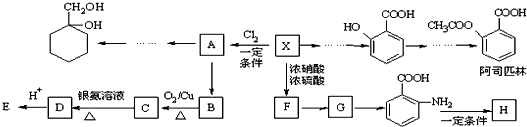
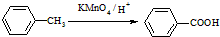
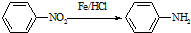 (苯胺,易被氧化)
(苯胺,易被氧化) ,F→G的反应类型是氧化反应.
,F→G的反应类型是氧化反应. .
.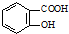 的同分异构体的结构简式
的同分异构体的结构简式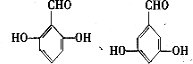 .(写出2种)
.(写出2种)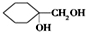 ,请设计合成路线,要求不超过4步(无机试剂任选).注:合成路线的书写格式参照如下示例流程图:
,请设计合成路线,要求不超过4步(无机试剂任选).注:合成路线的书写格式参照如下示例流程图: