题目内容
1.目前全球范围内环境污染备受关注,化工生产中应大力倡导“绿色化学”和“原子经济”的理念,工业生产中的废物利用尤为重要.工业上生产高氯酸时,还同时生产了一种常见的重要含氯消毒剂和漂白剂亚氯酸钠(NaClO2),其工艺流程如图: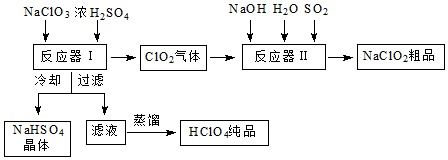
已知:①NaHSO4溶解度随温度的升高而增大,适当条件下可结晶析出.②高氯酸是至今为止人们已知酸中的最强酸,沸点90℃.请回答下列问题:
(1)反应器Ⅰ中发生反应的化学方程式为3NaClO3+3H2SO4=HClO4+2ClO2↑+3NaHSO4+H2O,冷却的目的是降低NaHSO4的溶解度,使NaHSO4结晶析出.
(2)反应器Ⅱ中发生反应的离子方程式为2ClO2+SO2+4OH-=2ClO2-+SO42-+2H2O.
(3)通入反应器Ⅱ中的SO2用H2O2代替同样能生成NaClO2,请简要说明双氧水在反应中能代替SO2的原因是H2O2有还原性也能把ClO2还原为NaClO2.
(4)Ca(ClO)2、ClO2、NaClO2等含氯化合物都是常用的消毒剂和漂白剂,是因为它们都具有强氧化性,请写出工业上用氯气和消石灰生产漂粉精的化学方程式:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O.
分析 NaClO3和浓H2SO4在反应器I中反应:3NaClO3+3H2SO4=HClO4+2ClO2↑+3NaHSO4+H2O;生成HClO4、ClO2和NaHSO4,ClO2在反应器II中与二氧化硫、氢氧化钠反应2ClO2+SO2+4NaOH═2NaClO2+Na2SO4+2H2O;生成亚氯酸钠,再得到其晶体;反应器I中得到的溶液通过冷却过滤得到NaHSO4晶体,滤液为HClO4,蒸馏得到纯净的HClO4.
(1)NaClO3和浓H2SO4在反应器I中反应生成HClO4、ClO2和NaHSO4;冷却溶液时会析出NaHSO4晶体;
(2)反应器Ⅱ中ClO2与二氧化硫、氢氧化钠反应生成亚氯酸钠;
(3)H2O2具有还原性,能还原ClO2;
(4)具有强氧化性的物质能用作消毒剂和漂白剂,氯气和消石灰反应生成氯化钙、次氯酸钙和水.
解答 解:(1)反应器Ⅰ中发生反应的化学方程式为3NaClO3+3H2SO4=HClO4+2ClO2↑+3NaHSO4+H2O;冷却溶液时会降低NaHSO4的溶解度,使NaHSO4结晶析出,
故答案为:3NaClO3+3H2SO4=HClO4+2ClO2↑+3NaHSO4+H2O;降低NaHSO4的溶解度,使NaHSO4结晶析出;
(2)反应器Ⅱ中ClO2与二氧化硫、氢氧化钠反应生成亚氯酸钠,其反应的离子方程式为:2ClO2+SO2+4OH-═2ClO2-+SO42-+2H2O,
故答案为:2ClO2+SO2+4OH-═2ClO2-+SO42-+2H2O;
(3)H2O2中O元素为-1价,有还原性,能被强氧化剂氧化,H2O2能还原ClO2,所以入反应器Ⅱ中的SO2用H2O2代替同样能生成NaClO2;
故答案为:H2O2有还原性也能把ClO2还原为NaClO2;
(4)具有强氧化性的物质能用作消毒剂和漂白剂,已知Ca(ClO)2、ClO2、NaClO2等含氯化合物都是常用的消毒剂和漂白剂,是因为它们都具有强氧化性;用氯气和消石灰生产漂粉精的化学方程式为2Cl2+2 Ca(OH )2=CaCl2+Ca(ClO)2+2H2O,
故答案为:强氧化性;2Cl2+2 Ca(OH )2=CaCl2+Ca(ClO)2+2H2O.
点评 本题考查物质的制备实验,为高频考点,把握制备流程中的反应、混合物分离提纯、元素和化合物知识、实验技能为解答的关键,侧重分析与实验能力的考查,题目难度中等.

| A. | 胶体就是直径为10-9m~10-7m的微粒 | |
| B. | 实验室制备Fe(OH)3胶体的方法是将饱和FeCl3溶液滴入NaOH溶液并加热 | |
| C. | 电解Fe(OH)3胶体,阴极附近红褐色加深,是因为胶体带正电,向阴极移动 | |
| D. | 可以用丁达尔效应来区别胶体和溶液 |
| A. | 离子半径:Z>W | |
| B. | 对应的氢化物的热稳定性:R>W | |
| C. | X与Z、W与Z均以原子个数比1:1形成的化合物中化学键类型不完全相同 | |
| D. | R的最高价氧化物的水化物与NaHYO3溶液反应有气泡生成,证明非金属性:R>Y |
| A. | 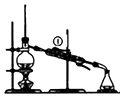 装置A可用于实验室制取蒸馏水,从①处通入冷却水 | |
| B. | 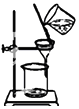 装置B可用于分离汽油和水,且汽油层由分液漏斗的下口放出 | |
| C. | 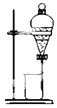 装置C可用于除去固体BaCl2中的BSaO4 | |
| D. |  装置D在配制一定物质的量浓度的溶液之前可以有水 |
| A. | K+、Fe3+、Cl- | B. | Na+、CO32-、H+ | C. | Na+、HCO3-、OH- | D. | K+、AlO2-、OH- |
①取少量该溶液,加入足量稀硫酸,无明显现象.
②取①反应后的溶液,加入足量浓NaOH溶液,最终得到红褐色沉淀,并伴有刺激性气味气体产生.
下列说法不正确的是( )
| A. | 根据实验①可知溶液中不存CO32-、SiO32- | |
| B. | 该溶液中肯定存在NH4+、Fe2+ | |
| C. | 该溶液中至少含有4种离子 | |
| D. | 另取该溶液,加入适量氯水和淀粉溶液,若溶液显蓝色,即可确定该溶液中只含NH4+、Fe2+、Fe3+、SO42-、I- |
| A. | 在标准状况下,1mol O2 与1mol 纯碱的体积相同 | |
| B. | 常温常压下,18g H2O所含的氧原子的数目为NA | |
| C. | 0.1mol Zn与含0.1mol HCl的盐酸充分反应,转移的电子数目为0.2NA | |
| D. | 1L 水溶解58.5g NaCl 所形成的溶液的物质的量浓度是0.1mol•L-1 |
| A. | 1.0 L 0.5mol/L的Na2SO4水溶液中含有的氧原子数为2NA | |
| B. | 用含有0.2mo1 FeCl3的饱和溶液配制的氢氧化铁胶体中,胶粒数等于0.2NA | |
| C. | 1.0g H2O与D2O的混合物所含中子数为0.5NA | |
| D. | 标准状况下,11.2L氯气与足量铁粉充分反应,转移的电予数为NA |