��Ŀ����
18��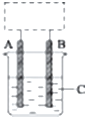 ijѧ���������ͼ��ʾ��װ�ã����ڲ���δ����������װ������������ķ�ӦΪCu+H2SO4�TH2��+CuSO4��δע����Ӧ���������Իش�
ijѧ���������ͼ��ʾ��װ�ã����ڲ���δ����������װ������������ķ�ӦΪCu+H2SO4�TH2��+CuSO4��δע����Ӧ���������Իش���1��A��B��������һ���ǽ���ͭ�������ƣ���������
�����������������������������������������
��2��д����װ���з�����ԭ��Ӧ�ĵ缫��Ӧ����ʽΪ2H++2e-=H2����
��3����C��ҺΪ100ml����ʳ��ˮ��A ��B�缫��Ϊ̼������ѧ������ͼʾװ���Լ��飨CH4������ȼ�ϵ��Ϊ��Դ���е�⣺
��д����Դ������ӦʽCH4-8e-+10OH-�TCO32-+7H2O��
�ڸõ������е��ܷ�Ӧ�����ӷ���ʽ2Cl-+2H2O$\frac{\underline{\;���\;}}{\;}$H2��+Cl2��+2OH-��
�۵������ų������112ml����ʱ���ñ���ʳ��ˮ��Һ��pH=13�������£�������������״�������Ϊ56mL��
���� ��1���÷�Ӧ�����Է����У�Ϊ�����У�Cu��������������ʯī���������������ӵ�Դ������
��2����װ���У������ϵõ��ӷ�����ԭ��Ӧ��
��3���ټ��������£�����ʧ��������̼������Ӻ�ˮ��
����ʯī���缫��ⱥ���Ȼ�����Һʱ�������������ӷŵ硢�����������ӷŵ磬ͬʱ�����������������������ɣ�
�۸�������������������֮��Ĺ�ϵ��������������Ũ�ȣ��Ӷ�������Һ��pH�����ݵ����غ����������
��� �⣺��1����װ������������ķ�ӦΪCu+H2SO4�TH2��+CuSO4���÷�Ӧ�����Է����У�Ϊ���أ�Cu��������������ʯī��������Cu���ӵ�Դ������������
�ʴ�Ϊ��ͭ��������
��2����װ���У������������ӵõ��ӷ�����ԭ��Ӧ���缫��ӦʽΪ2H++2e-=H2����
�ʴ�Ϊ��2H++2e-=H2����
��3���ټ��������£�����ʧ��������̼������Ӻ�ˮ�����ĵ缫����ʽΪ��CH4-8e-+10OH-�TCO32-+7H2O��
�ʴ�Ϊ��CH4-8e-+10OH-�TCO32-+7H2O��
����ʯī���缫��ⱥ���Ȼ�����Һʱ�������������ӷŵ����������������������ӷŵ�����������ͬʱ�����������������������ɣ���ط�ӦʽΪ2Cl-+2H2O$\frac{\underline{\;���\;}}{\;}$H2��+Cl2��+2OH-��
�ʴ�Ϊ��2Cl-+2H2O$\frac{\underline{\;���\;}}{\;}$H2��+Cl2��+2OH-��
����ʯī���缫��ⱥ���Ȼ�����Һʱ�������������ӷŵ����������������������ӷŵ�����������ͬʱ�����������������������ɣ���ط�ӦʽΪ2Cl-+2H2O$\frac{\underline{\;���\;}}{\;}$H2��+Cl2��+2OH-��
���������������ӵ����ʵ���Ϊx��
2Cl-+2H2O$\frac{\underline{\;���\;}}{\;}$H2��+Cl2��+2OH-��
22.4L 2mol
0.112L x
22.4L��2mol=0.112L��x��
x=$\frac{0.112L��2mol}{22.4L}$=0.01mol��
c��OH-��=$\frac{0.01mol}{0.1L}$=0.1mol/L������Һ��pH=13��
���ʱת�Ƶ��ӵ����ʵ����������������ӵ����ʵ�������ת�Ƶ���Ϊ0.01mol����2O2+8e-+4H2O�T8OH-��֪����������Ϊ0.0025mol��������ڱ�״����Ϊ56mL��
�ʴ�Ϊ��2Cl-+2H2O$\frac{\underline{\;���\;}}{\;}$2OH_+H2��+Cl2����13��56��
���� ���⿼��ԭ��غ͵���ԭ�������ݷ���ʽ���Է����жϵ�����ͣ�֪��ԭ��غ͵��ص����𣬻���д�缫��Ӧʽ���ѵ���pH�ļ��㣬��Ŀ�Ѷ��еȣ������ڿ���ѧ���ķ��������ͼ���������

| A�� | NaCl�ĵ���ʽ��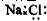 | B�� | N2�Ľṹʽ��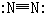 | C�� | NH4Cl�ĵ���ʽΪ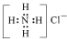 | D�� | F-�Ľṹʾ��ͼ��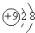 |
| A�� | Al3+��NH4+��SO42-��Cl- | B�� | K+��Fe2+��MnO4-��Cl- | ||
| C�� | NH4+��SiO32-��NO3-��K+ | D�� | Na+��K+��HCO3-��Mg2+ |
| A�� | �����۵��ɵ͵��ߣ�CCl4��CBr4��CI4��CF4 | |
| B�� | �������ɴ�С��NaF��NaCl��NaBr��NaI | |
| C�� | �۵��ɸߵ��ͣ�Na��Mg��Al | |
| D�� | Ӳ���ɴ�С�����ʯ������裾̼���� |
| A�� | ��NaCl��Һ��NaOH��ҺΪ���Һʱ��������Ӧ��ΪO2+2H2O+4e-�T4OH- | |
| B�� | ��NaOH��ҺΪ���Һʱ��������ӦΪAl+3OH--3e-�TAl��OH��3 | |
| C�� | ��NaOH��ҺΪ���Һʱ������ڹ��������е��Һ�ļ��Ա��ֲ��� | |
| D�� | ��ع���ʱ������3mol����ͨ�����·ʱ������16.8LO2 |
 ��
��