题目内容
下列各指定微粒的数目不等于阿伏加德罗常数的是( )
| A、2g氢气所含的原子数 |
| B、4g氦气所含的原子数 |
| C、12.6g HNO3所含的原子数 |
| D、0.5mol氧气所含的原子数 |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:12g碳-12中含有的碳原子数为阿伏伽德罗常数,即粒子的物质的量为1mol时,含有相应粒子数为阿伏伽德罗常数;将各选项中的物理量转化成物质的量,物质的量为1mol即可满足条件.
解答:
解:A.2g氢气的物质的量为:
=1mol,1mol氢气中含有2mol氢原子,含有2NA个氢原子,含有的原子数不等于阿伏伽德罗常数,故A正确;
B.4g氦气的物质的量为:
=1mol,1mol氦气中含有1mol氦原子,含有阿伏伽德罗常数个原子,故B错误;
C.12.6g硝酸的物质的量为:
=0.2mol,含有原子的物质的量为:0.2mol×(1+1+3)=1mol,含有阿伏伽德罗常数个原子,故C错误;
D.0.5mol氧气中含有氧原子的物质的量为1mol,含有阿伏伽德罗常数个O原子,故D错误;
故选A.
| 2g |
| 2g/mol |
B.4g氦气的物质的量为:
| 4g |
| 4g/mol |
C.12.6g硝酸的物质的量为:
| 12.6g |
| 63g/mol |
D.0.5mol氧气中含有氧原子的物质的量为1mol,含有阿伏伽德罗常数个O原子,故D错误;
故选A.
点评:本题考查阿伏加德罗常数的判断,题目难度不大,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系,明确阿伏伽德罗常数的概念为解答本题的关键.

练习册系列答案
相关题目
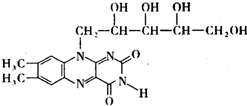 含工业染色剂“苏丹红一号”的有毒食品曾流入市场,引起人们的恐慌.研究表明:核黄素(即维生素B2)能缓解“苏丹红一号”的毒性,其结构如图下列有关核黄素的说法中,正确的是( )
含工业染色剂“苏丹红一号”的有毒食品曾流入市场,引起人们的恐慌.研究表明:核黄素(即维生素B2)能缓解“苏丹红一号”的毒性,其结构如图下列有关核黄素的说法中,正确的是( )| A、核黄素属于分子晶体 |
| B、核黄素能发生银镜反应 |
| C、核黄素属于糖类 |
| D、核黄素不能被酸性高锰酸钾溶液氧化 |
一元酸HA溶液中,加入一定量强碱MOH溶液后,恰好完全反应,反应后的溶液中,下列判断正确的是( )
| A、c(A-)≥c(M+) |
| B、c(A-)≤c(M+) |
| C、c(OH-)<c(A-) |
| D、若MA水解,则c(OH-)>c(A-) |
对于2KI+Br2=2KBr+I2和2HBrO3+I2=2HIO3+Br2两反应,下列叙述不正确的是( )
| A、Br2的氧化性强于I2氧化性 | ||||
| B、I-的还原性强于Br-的还原性 | ||||
| C、I2的氧化性强于Br2的氧化性 | ||||
D、BrO
|
由A、B两种气体组成的混合气体(A、B的相对分子质量分别为MA和MB),若A的质量分数为W%,则混合气体的平均相对分子质量是( )
A、
| ||||||
B、
| ||||||
| C、MA?W%+MB(1-W%) | ||||||
| D、无法确定 |
有8种物质:①甲烷;②苯;③聚乙烯;④邻二甲苯; ⑤乙炔; 既能使酸性高锰酸钾溶液褪色又能与溴水反应使之褪色的是( )
| A、③④⑤ | B、④⑤ |
| C、只有⑤ | D、全部 |
