题目内容
12.下列反应的离子方程式正确的是( )| A. | 向碳酸氢铵溶液中加入足量的氢氧化钠溶液:HCO3-+OH-═CO32-+H2O | |
| B. | 向Ba(OH)2溶液中滴加NaHSO4溶液至恰好为中性:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| C. | 用酸化的高锰酸钾溶液氧化双氧水:2MnO4-+6H++5H2O2═2Mn2++5O2↑+8H2O | |
| D. | Ca(ClO)2溶液中通入过量的二氧化硫气体:ClO-+SO2+H2O═HClO+HSO3- |
分析 A.漏写铵根离子与碱的反应;
B.反应生成硫酸钠、硫酸钡和水;
C.发生氧化还原反应,遵循电子、电荷守恒;
D.发生氧化还原反应生成硫酸钙.
解答 解:A.向碳酸氢铵溶液中加入足量的氢氧化钠溶液的离子反应为NH4++HCO3-+2OH-═NH3•H2O+CO32-+H2O,故A错误;
B.向Ba(OH)2溶液中滴加NaHSO4溶液至恰好为中性的离子反应为Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O,故B错误;
C.用酸化的高锰酸钾溶液氧化双氧水的离子反应为2MnO4-+6H++5H2O2═2Mn2++5O2↑+8H2O,故C正确;
D.次氯酸钙溶液中通入过量的二氧化硫气体的离子反应为2ClO-+2H2O+Ca2++2SO2═CaSO4↓+SO42-+4H++Cl-,故D错误;
故选C.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应、氧化还原反应的离子反应考查,注意离子反应中保留化学式及电子、电荷守恒,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
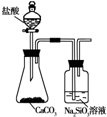
2.某研究性学习小组设计如图装置制取氯气并检验氯气的某些性质.
(1)制取Cl2,检验干燥氯气是否有漂白性.
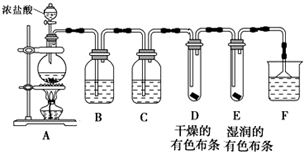
①盛装浓盐酸的仪器的名称是分液漏斗,烧瓶中发生反应的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O
②B中盛有饱和食盐水,其作用是除去Cl2中混有的HCl,C中盛装的试剂是浓硫酸
③通入Cl2后,D、E中观察到的现象是中布条不褪色,E中布条褪色;根据现象可得出的结论是干燥的Cl2没有漂白性.
④F中盛有NaOH溶液,其作用是吸收氯气,防止环境污染,若有2.24L(标准状况下)Cl2被NaOH溶液完全吸收,则反应过程中转移的电子为0.1mol.
(2)探究铁丝在Cl2中燃烧的产物
某同学认为,当足量Cl2与少量铁丝反应时生成FeCl3,当少量Cl2与足量铁丝反应时生成FeCl2.为检验该观点是否正确,该同学将一根细的纯铁丝分别在足量和少量的Cl2中点燃,取其表面生成物配制成溶液A、B,并取溶液进行以下实验,请填写下表中的空格.
④根据实验结论,铁丝在Cl2中点燃的化学方程式:2Fe+3Cl2$\frac{\underline{\;点燃\;}}{\;}$2FeCl3 .
(1)制取Cl2,检验干燥氯气是否有漂白性.

①盛装浓盐酸的仪器的名称是分液漏斗,烧瓶中发生反应的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O
②B中盛有饱和食盐水,其作用是除去Cl2中混有的HCl,C中盛装的试剂是浓硫酸
③通入Cl2后,D、E中观察到的现象是中布条不褪色,E中布条褪色;根据现象可得出的结论是干燥的Cl2没有漂白性.
④F中盛有NaOH溶液,其作用是吸收氯气,防止环境污染,若有2.24L(标准状况下)Cl2被NaOH溶液完全吸收,则反应过程中转移的电子为0.1mol.
(2)探究铁丝在Cl2中燃烧的产物
某同学认为,当足量Cl2与少量铁丝反应时生成FeCl3,当少量Cl2与足量铁丝反应时生成FeCl2.为检验该观点是否正确,该同学将一根细的纯铁丝分别在足量和少量的Cl2中点燃,取其表面生成物配制成溶液A、B,并取溶液进行以下实验,请填写下表中的空格.
| 实验方法 | 实验现象 | 结论 |
| 分别向A、B溶液中滴加2滴①KSCN溶液 | ②两份溶液都变血红色 | 生成物中都有FeCl3 |
| 分别向A、B溶液中滴加几滴KMnO4溶液 | 两份溶液颜色均无明显变化 | 生成物中都不含③FeCl2 |
3.抗酸药是一类能中和胃酸过多的药物.下列不能作为抗酸药有效成分的是( )
| A. | NaHC03 | B. | CaC03 | C. | Al(OH)3 | D. | NaOH |
20.硅及其化合物的应用范围很广.下列说法正确的是( )
| A. | 硅是人类将太阳能转换为电能的常用材料 | |
| B. | 单质硅是制光导纤维的材料 | |
| C. | 粗硅制备高纯度单质硅不涉及氧化还原反应 | |
| D. | 硅能与氢氟酸反应,则硅可以与盐酸反应 |
7.化学与社会、生产、生活密切相关.下列说法正确的是( )
| A. | 用硫磺熏蒸使银耳增白 | |
| B. | 用废旧皮革生产药用胶囊可以提高原子利用率 | |
| C. | 用明矾对自来水进行杀菌消毒 | |
| D. | 限制使用一次性塑料制品的主要目的是防止形成“白色污染” |
4.工业上,将氨气和空气的混合气体通过灼热铂-铑合金网,发生氨氧化反应.若有标准状况下aL氨气完全反应,并转移了b个电子,则阿伏伽德罗常数NA的数值可表示为( )
| A. | $\frac{22.4b}{5a}$ | B. | $\frac{5a}{11.2b}$ | C. | $\frac{22.4a}{5b}$ | D. | $\frac{11.2b}{5a}$ |
1.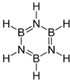 互为等电子体的物质具有相似的结构特征和化学性质.B3N3H6与C6H6(苯)互为等电子体,则关于B3N3H6的说法错误的是( )
互为等电子体的物质具有相似的结构特征和化学性质.B3N3H6与C6H6(苯)互为等电子体,则关于B3N3H6的说法错误的是( )
 互为等电子体的物质具有相似的结构特征和化学性质.B3N3H6与C6H6(苯)互为等电子体,则关于B3N3H6的说法错误的是( )
互为等电子体的物质具有相似的结构特征和化学性质.B3N3H6与C6H6(苯)互为等电子体,则关于B3N3H6的说法错误的是( )| A. | 其二氯代物有3种同分异构体 | B. | 能发生加成反应和取代反应 | ||
| C. | 不能使酸性KMnO4溶液褪色 | D. | 所有原子都在同一平面上 |