题目内容
下列叙述中正确的是( )
| A、氯气的水溶液可以导电,说明氯气是电解质 | B、漂白粉和明矾都常用于处理自来水,二者的作用原理是相同的 | C、氯气可以使湿润的有色布条褪色,起漂白作用的物质是次氯酸 | D、滴有酚酞的Na2CO3溶液中加入足量BaCl2后,溶液保持红色并产生沉淀 |
分析:A.氯气为单质,电解质必须是混合物;
B.漂白粉具有强氧化性,可杀菌消毒,明矾水解生成具有吸附性的氢氧化铝,可除去水中的悬浮物;
C.氯气和水反应生成具有漂白性的次氯酸;
D.Na2CO3水解呈碱性,加入足量BaCl2后,溶液褪色.
B.漂白粉具有强氧化性,可杀菌消毒,明矾水解生成具有吸附性的氢氧化铝,可除去水中的悬浮物;
C.氯气和水反应生成具有漂白性的次氯酸;
D.Na2CO3水解呈碱性,加入足量BaCl2后,溶液褪色.
解答:解:A.氯气是单质,既不是电解质也不是非电解质,本身不能电离,故A错误;
B.漂白粉净水是利用其氧化性,明矾净水是利用胶体的吸附性,故B错误;
C.氯气和水反应生成次氯酸,次氯酸具有漂白性,氯气不具有漂白性,故C正确;
D.碳酸根离子与钡离子作用生成碳酸钡沉淀,碳酸根离子的水解平衡左移,氢氧根离子浓度降低,故红色变浅或褪去,故D错误.
故选C.
B.漂白粉净水是利用其氧化性,明矾净水是利用胶体的吸附性,故B错误;
C.氯气和水反应生成次氯酸,次氯酸具有漂白性,氯气不具有漂白性,故C正确;
D.碳酸根离子与钡离子作用生成碳酸钡沉淀,碳酸根离子的水解平衡左移,氢氧根离子浓度降低,故红色变浅或褪去,故D错误.
故选C.
点评:本题考查较为综合,涉及氯气的性质、电解质、盐类的水解等问题,侧重于元素化合物知识的综合运用,为高考常见题型,难度不大,注意相关基础知识的积累.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
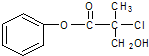 有机物A是农药生产中的一种中间体,结构简式如图所示.下列叙述中正确的是( )
有机物A是农药生产中的一种中间体,结构简式如图所示.下列叙述中正确的是( )| A、有机物A可以在一定条件下与HBr发生反应 | B、1mol A最多能与4mol H2发生加成反应 | C、有机物A与浓硫酸混合加热,可以发生消去反应 | D、1mol A与足量的NaOH溶液反应,最多可以消耗3mol NaOH |


