题目内容
16.下列除杂方案合理的是( )| A. | 除去苯中的少量苯酚:加浓溴水,过滤 | |
| B. | 除去乙酸乙酯中的少量乙酸:加入饱和Na2CO3溶液,过滤 | |
| C. | 除去甲醛中少量的乙烯:通过盛有溴水的洗气瓶,洗气 | |
| D. | 除去溴苯中少量的Br2:加入稍过量氢氧化钠,分液 |
分析 A.三溴苯酚溶于苯;
B.乙酸乙酯不溶于饱和碳酸钠溶液,乙酸与碳酸钠反应;
C.甲醛、乙烯都与溴水反应;
D.溴苯不溶于水,与氢氧化钠溶液不反应.
解答 解:A.苯酚与溴水反应生成三溴苯酚,三溴苯酚溶于苯,不能除杂,应用氢氧化钠溶液,故A错误;
B.乙酸乙酯不溶于饱和碳酸钠溶液,乙酸与碳酸钠反应,可用于除杂,但应用分液的方法,故B错误;
C.甲醛、乙烯都与溴水反应,不能用于除杂,故C错误;
D.溴苯不溶于水,与氢氧化钠溶液不反应,而溴与氢氧化钠溶液反应,可用于除杂,故D正确.
故选D.
点评 本题考查混合物分离、提纯的方法及选择,为高频考点,把握物质的性质及性质差异、混合物分离方法为解答的关键,注重实验基础知识和基本技能的考查,注意有机物性质,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
7.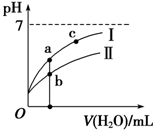 已知:25℃时某些弱酸的电离平衡常数.下面图象表示常温下稀释CH3COOH、HClO两种酸的稀溶液时,溶液pH随加水量的变化,下列说法正确的是( )
已知:25℃时某些弱酸的电离平衡常数.下面图象表示常温下稀释CH3COOH、HClO两种酸的稀溶液时,溶液pH随加水量的变化,下列说法正确的是( )
 已知:25℃时某些弱酸的电离平衡常数.下面图象表示常温下稀释CH3COOH、HClO两种酸的稀溶液时,溶液pH随加水量的变化,下列说法正确的是( )
已知:25℃时某些弱酸的电离平衡常数.下面图象表示常温下稀释CH3COOH、HClO两种酸的稀溶液时,溶液pH随加水量的变化,下列说法正确的是( )| CH3COOH | HClO | H2CO3 |
| Ka=1.8×10 -5 | Ka=3.0×10 -8 | Ka1=4.1×10 -7 Ka2=5.6×10 -11 |
| A. | 相同浓度CH3COONa和NaClO的混合液中,各离子浓度大小关系为:c(Na+)>c(ClO-)>c(CH3COO-)>c(OH-)>c(H+) | |
| B. | 向NaClO溶液中通少量CO2的离子方程式为:2ClO-+CO2+H2O=2HClO+CO32- | |
| C. | 图象中a、c两点处的溶液中$\frac{c(R-)}{c(HR)•c(OH-)}$相等(HR代表CH3COOH或HClO) | |
| D. | 图象中a点酸的总浓度等于b点酸的总浓度 |
4.正逆反应的反应速率-时间、转化率-时间关系图如下:则下列分析中不正确的是( )
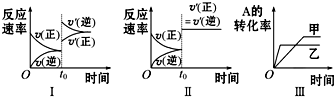

| A. | 图Ⅰ可体现t0时升高温度对反应速率的影响 | |
| B. | 图Ⅱ可体现t0时增大压强(缩小体积)或使用催化剂对反应速率的影响 | |
| C. | 图Ⅲ可体现催化剂对化学平衡的影响,且甲使用了催化剂 | |
| D. | 图Ⅲ可体现温度对化学平衡的影响,且乙的温度较高 |
11.下列鉴别方法不能达到实验目的是( )
| A. | 用激光笔鉴别淀粉溶液与氯化钠溶液 | |
| B. | 用KOH溶液鉴别NH4Cl、AlCl3、MgSO4、FeCl3四种溶液 | |
| C. | 用盐酸溶液鉴别Na2CO3溶液和Na2SiO3溶液 | |
| D. | 用BaCl2溶液鉴别AgNO3和Na2SO4 |
1.分类是学习和研究化学的一种重要方法,下列分类合理的是( )
| A. | 纯碱属于碱 | B. | 小苏打不属于电解质 | ||
| C. | 水玻璃属于纯净物 | D. | CO不属于酸性氧化物 |
8.下列叙述中正确的是( )
| A. | 1 mol CO2的体积是22.4L | B. | 1 mol NaCl的质量是58.5 | ||
| C. | H2SO4的摩尔质量是98 g/mol | D. | 1 mol/L NaOH溶液中含有1 molNa+ |
5. 纳米级二氧化锰的活性很高,以二氧化锰为电极构成的燃料电池如图所示.下列说法不正确的是 ( )
纳米级二氧化锰的活性很高,以二氧化锰为电极构成的燃料电池如图所示.下列说法不正确的是 ( )
 纳米级二氧化锰的活性很高,以二氧化锰为电极构成的燃料电池如图所示.下列说法不正确的是 ( )
纳米级二氧化锰的活性很高,以二氧化锰为电极构成的燃料电池如图所示.下列说法不正确的是 ( )| A. | a极为正极,发生还原反应 | |
| B. | b极的电极反应式为(CH2O)n-4ne-+n H2O=nCO2+4n H+ | |
| C. | 电子由b极流出经用电器流向a极 | |
| D. | 放电时H+由质子交换膜左侧向右侧迁移 |
 有效地利用现有新能源和开发新能源已受到各国的重视.
有效地利用现有新能源和开发新能源已受到各国的重视.