题目内容
18.下列说法正确的是( )| A. | 1 mol H2的质量只有在标准状况下才为2 g | |
| B. | 标准状况下,1 mol水蒸气的体积大约为22.4 L | |
| C. | 273℃,1.01×105 Pa状态下,1 mol气体体积大于22.4 L | |
| D. | 0.5 mol O2和0.5 mol N2组成的混合气体体积约为22.4 L |
分析 A.根据m=nM计算出氢气质量,物质质量与物质所处状态无关;
B.标准状况下,水的状态不是气态;
C.温度升高,气态体积增大,结合标准状况下1mol气态体积约为22.4L计算;
D.没有指出在标准状况下,不能使用22.4L/mol计算.
解答 解:A.1mol氢气的质量为:2g/mol×1mol=2g,无论在什么条件下1mol氢气的质量都是2g,故A错误;
B.标准状况下水的状态不是气态,不能使用标准状况下的气体摩尔体积计算,故B错误;
C.273℃,1.01×105 Pa状态下的温度高于标准状况下,则该条件下气体摩尔体积大于22.4L/mol,1mol气态在该条件下体积大于22.4L,故C正确;
D.不是标准状况下,不能使用标准状况下的气体摩尔体积计算混合气体的体积,故D错误;
故选C.
点评 本题考查了物质的量的计算,题目难度不大,明确标准状况下气体摩尔体积的使用条件为解答关键,注意掌握物质的量与摩尔质量、气体摩尔体积之间的关系,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案 新思维寒假作业系列答案
新思维寒假作业系列答案
相关题目
8. 2010年上海世博会的主题是“城市,让生活更美好”.大会提倡低碳、节能、环保,下列叙述正确的是( )
2010年上海世博会的主题是“城市,让生活更美好”.大会提倡低碳、节能、环保,下列叙述正确的是( )
 2010年上海世博会的主题是“城市,让生活更美好”.大会提倡低碳、节能、环保,下列叙述正确的是( )
2010年上海世博会的主题是“城市,让生活更美好”.大会提倡低碳、节能、环保,下列叙述正确的是( )| A. | 中国馆--“东方之冠”使用的钢筋混凝土属于合金 | |
| B. | 制作快餐饭盒的可降解“玉米塑料”(主要成分为聚乳酸)是纯净物 | |
| C. | 英国馆--“种子圣殿”,由多根亚克力[分子式(C5H8O2)]杆构建而成,亚克力属于烃 | |
| D. | 光伏发电技术的核心材料--晶体硅属于原子晶体 |
9.下列各组物质中属于同分异构体的是( )
| A. | 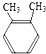 和 和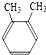 | B. | CH3CH2OH 和 CH3 CH2-O-CH2CH3 | ||
| C. | 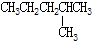 和 和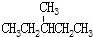 | D. | 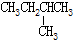 和 和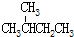 |
3.鉴别①NaOH;②Al2(SO4)3;③Ba(NO3)2;④FeCl3;⑤KCl五种溶液,不用其它试剂,被鉴别出来的顺序是( )
| A. | ①②③④⑤ | B. | ④③①②⑤ | C. | ④①②③⑤ | D. | ②③①④⑤ |
10.电解质在溶液中的行为是化学研究的重要内容.下列有关溶液的叙述正确的是( )
| A. | 常温下 pH为5的盐酸溶液稀释 1000倍后,pH 等于8 | |
| B. | 在滴有酚酞溶液的氨水里,加入盐酸至恰好呈无色,则此时溶液的 pH=7 | |
| C. | 浓度均为0.1 mol/L的氨水和氯化铵溶液,水电离出的 c(H+)前者大于后者 | |
| D. | 等浓度的 CH3COOH与 KOH任意比混合:c(K+)+c(H+)=c(OH-)+c(CH3COO-) |
7.下列说法符合汤姆孙原子结构模型的观点是( )
①任何原子都是电中性的;
②原子像带正电的海洋,电子漂在正电荷的海洋中;
③原子是由带正电的物质和电子构成的;
④阴极射线产生的原因是电子很小,在原子受打击时电子就容易跑出去.
①任何原子都是电中性的;
②原子像带正电的海洋,电子漂在正电荷的海洋中;
③原子是由带正电的物质和电子构成的;
④阴极射线产生的原因是电子很小,在原子受打击时电子就容易跑出去.
| A. | ①②④ | B. | ① | C. | ①②③ | D. | ①②③④ |
8.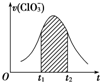 氯酸钾和亚硫酸氢钾能发生氧化还原反应:ClO3-+HSO3-→SO42-+Cl-+H+(未配平).已知该反应的速率随c(H+)的增大而加快.如图为用ClO3-在单位时间内物质的量浓度变化表示的该反应v-t图.下列说法中不正确的是( )
氯酸钾和亚硫酸氢钾能发生氧化还原反应:ClO3-+HSO3-→SO42-+Cl-+H+(未配平).已知该反应的速率随c(H+)的增大而加快.如图为用ClO3-在单位时间内物质的量浓度变化表示的该反应v-t图.下列说法中不正确的是( )
 氯酸钾和亚硫酸氢钾能发生氧化还原反应:ClO3-+HSO3-→SO42-+Cl-+H+(未配平).已知该反应的速率随c(H+)的增大而加快.如图为用ClO3-在单位时间内物质的量浓度变化表示的该反应v-t图.下列说法中不正确的是( )
氯酸钾和亚硫酸氢钾能发生氧化还原反应:ClO3-+HSO3-→SO42-+Cl-+H+(未配平).已知该反应的速率随c(H+)的增大而加快.如图为用ClO3-在单位时间内物质的量浓度变化表示的该反应v-t图.下列说法中不正确的是( )| A. | 反应开始时速率增大可能是c(H+)所致 | |
| B. | 后期反应速率下降的主要原因是反应物浓度减小 | |
| C. | 纵坐标为v(H+)的v-t曲线与图中曲线完全重合 | |
| D. | 图中阴影部分“面积”可以表示t1-t2时间为c(Cl-)增加 |
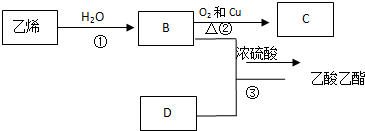
 ,空间构型为平面形.
,空间构型为平面形.