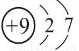题目内容
某磁黄铁矿的主要成分是FexS(S为一2价),既含有Fe2+又含有Fe3+。将一定量的该磁黄铁矿与100mL的盐酸恰好完全反应(注:矿石中其他成分不与盐酸反应),生成硫单质2.4 g、FeCl2 0.425 mol和一定量H2S气体,且溶液中无Fe3+。则下列说法正确的是
A.100 mL的盐酸中HC1物质的量浓度为7.5 mol/L
B.生成的H2S气体在标准状况下的体积为2.24 L
C.该磁黄铁矿FexS中,Fe2+与Fe3+的物质的量之比为3 : 1
D.该磁黄铁矿中FexS的x=0.85
钴(Co)及其化合物在工业上有广泛应用。为从某工业废料中回收钴,某学生设计流程如下(废料中含有Al、Li、Co2O3和Fe2O3等物质)。
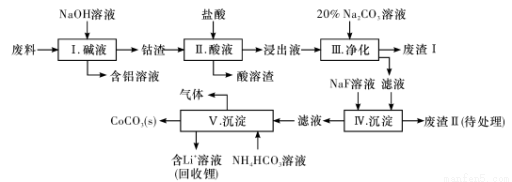
已知:①物质溶解性:LiF、CoCO3难溶于水,Li2CO3微溶于水;
② Co2O3有强氧化性,能氧化盐酸;
③ 部分金属离子形成氢氧化物沉淀的pH见下表:
Fe3+ | Co2+ | Co3+ | Al3+ | |
pH(开始沉淀) | 1.9 | 7.15 | -0.23 | 3.4 |
pH(完全沉淀) | 3.2 | 9.15 | 1.09 | 4.7 |
请回答:
(1) 步骤I中得到含铝溶液的反应的离子方程式是________________。
(2) 步骤D中加人盐酸的作用是________________。
(3) 步骤III中Na2CO3溶液的作用是调节溶液的PH,应使溶液的pH控制在_____(填范围),废渣I中的成分有________________。
(4) 步骤V中产生CoCO3的离子方程式是________________。
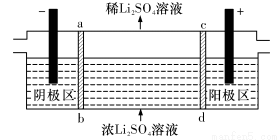
(5) 滤渣II用硫酸处理后用三室式电渗析法电解可得LiOH溶液和稀硫酸。则离子交换膜c为__________(填“阴”或“阳”)离子交换膜,随着电解的进行,阴极区pH将_________(填“增大”、“减小”或“不变”)。
(6) 向所得LiOH溶液中加入NH4HCO3即可得到Li2CO3。工业上以碳酸锂和碳酸钴在空气中高温煅烧制备锂离子电池的正极材料钴酸锂 (LiCoO2)时,还会产生一种三原子构成的直线型气体分子,该分子的电子式为_______________,写出工业上用上述方法制备钴酸锂的化学反应方程式___________________。
(7) 某锂离子充电时电池的总反应为C6+ LiCoO2==LixC6+Li1-xCoO2,该锂离子电池放电时正极的电极反应式为__________________。



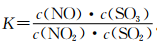 。恒容时,温度升高,NO浓度减小。下列说法不正确的是
。恒容时,温度升高,NO浓度减小。下列说法不正确的是 NO+SO3
NO+SO3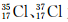 为不同的核素,有不同的化学性质
为不同的核素,有不同的化学性质