题目内容
第四周期基态原子第四能层的各能级电子数之和为奇数的元素共有( )
| A、2种 | B、4种 | C、6种 | D、8种 |
考点:原子核外电子排布
专题:
分析:第四周期基态原子第四能层的各能级电子数之和为奇数的元素分别为4s1,4s24p1,4s24p3,4s24p5,3d104s1、3d54s1,六种元素.
解答:
解:第四周期基态原子第四能层的各能级电子数之和为奇数的元素分别为4s1,4s24p1,4s24p3,4s24p5,3d104s1、3d54s1,六种元素,故答案为:C.
点评:本题考查核外电子排布,比较基础,学生容易忽略过渡元素,关键是对核外电子排布规律的理解掌握.

练习册系列答案
相关题目
莫尔盐[(NH4)2Fe(SO4)2?6H2O]常作氧化还原滴定的基准物质,在1L 0.1mol/L的该盐溶液中,下列有关比较正确的是( )
| A、c(NH4+)+c(NH3?H2O)=0.1 mol/L |
| B、2c(Fe2+)+c(NH4+)=2c(SO42-) |
| C、c(SO42-)>c(NH4+)>c(Fe2+)>c(H+)>c(OH-) |
| D、c(NH4+):c(Fe2+):c(SO42-)=2:1:2 |
下列变化能用勒夏特列原理解释的是( )
| A、工业生产合成氨时一般选择在500℃的温度下进行 |
| B、H2、I2、HI混合气体加压后颜色变深 |
| C、合成氨时采用循环操作,可提高原料的利用率 |
| D、红棕色的NO2加压后颜色先变深再变浅 |
反应2A+3B=C+2D在2L的密闭容器中进行,半分钟后,C的物质的量增加了0.3mol,则此反应的平均速率表达正确的是( )
| A、v(C)=0.01 mol?L-1?s-1 |
| B、v(B)=0.03 mol?L-1?s-1 |
| C、v(A)=0.01 mol?L-1?s-1 |
| D、v(D)=0.02 mol?L-1?s-1 |
下列四组物质间的反应,有一组反应中的水与其他三组有本质不同的是( )
| A、Cl2+H2O═HCl+HclO |
| B、2F2+2H2O═4HF+O2 |
| C、3NO2+H2O═2HNO3+NO |
| D、2Na2O2+2H2O═4NaOH+O2↑ |
X、Y、Z是分别位于不同周期的三种短周期元素,且原子序数逐渐增大,X、Z属于同一主族,三种元素可以形成原子个数比为1:1:1的化合物W.下列推测正确的是( )
| A、元素Z的氧化物一定属于碱性氧化物 |
| B、原子半径关系是:X<Y<Z |
| C、三种元素中,Y的金属性最强 |
| D、Y、Z都能形成含氧酸,且前者的酸性比后者酸性强 |
与4.4g二氧化碳所含原子数相同的一氧化碳的质量是( )
| A、1.5 g |
| B、3.0 g |
| C、4.2 g |
| D、9.0 g |
下列物质的分类合理的是( )
| A、酸性氧化物:Na2O、CaO、CuO |
| B、碱:烧碱、纯碱、苛性钾 |
| C、盐:NH4Cl、NH4NO3、(NH4)2SO4、NH3?H2O |
| D、氧化物:CO2、NO、SO2、H2O |
 可以用键线式简单表示为
可以用键线式简单表示为 .则下列与X互为同分异构体的是
.则下列与X互为同分异构体的是
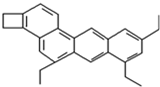
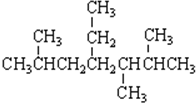 (按系统命名法)名称为
(按系统命名法)名称为