题目内容
6.请根据H、O、Na、Si、S、Cl、Fe、Cu八种元素及其化合物,并用化学用语回答下列问题:(1)写出元素O的离子结构示意图
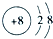 .
.(2)写出元素Na与S形成化合物的电子式是
 .
.(3)写出元素O、Na、S的离子半径由大到小的顺序为r(S2-)>r(O2-)>r(Na+).
(4)写出元素Si、S、Cl最高价氧化物由强到弱的顺序为HClO4>H2SO4>H2SiO3.
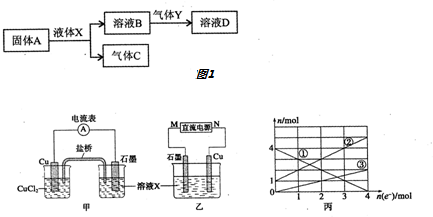
(5)由上述部分元素组成的物质间,在一定条件下,可以发生如图1所示的变化,其中A是一种淡黄色的固体,请回答:
①写出固体A与液体X反应的离子方程式2Na2O2+2H2O═4Na++OH-+O2↑.
②Y是一种形成酸雨气体.可用溶液B吸收,当B与Y物质的量之比为1:1且恰好完全反应时,所得溶液D.已知溶液D显酸性,则D溶液中各种离子浓度由大到小的顺序为c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>c(OH-).
(6)某反应中反应物与生成物有FeCl2、FeCl3、CuCl2、Cu.上述反应设计成的原电池如图甲所示,设计成的电解池如图乙所示,乙烧杯中金属阳离子的物质的量与电子转移的物质的量的变化关系如图丙.
①图中X溶液是FeCl3和FeCl2;
②原电池工作时,盐桥中的K+(选填“K+”或“Cl-”)不断进入X溶液中
③图丙中的②线是Fe2+的变化.
④当电子转移2mol时,向乙烧杯中加入2.8L5mol•L-1NaOH溶液才能使有的金属阳离子沉淀完全.
分析 (1)氧离子核内有8个质子,核外有两个电子层,分别容纳2,8个电子
(2)硫化钠中存在钠离子和硫离子,钠离子直接用离子符号表示,硫离子需要标出最外层电子及所带电荷;
(3)电子层结构相同的离子,离子半径随着原子序数增大而减小;电子层不同的离子半径随电子层数的增多而增大;
(4)元素的非金属性越强,对应的最高价氧化物对应的水化合物酸性越强,本题要首先判断元素的非金属性强弱;
(5)由题干可知:淡黄色固体A是Na2O2;液体X是H2O;气体Y是SO2;气体C则为O2;溶液D显酸性是NaHSO3;
(6)①该反应为2FeCl3+Cu═2FeCl2+CuCl2,Cu做负极,石墨为正极,X为FeCl3和FeCl2溶液;
②盐桥中阳离子向正极移动
③根据转移电子的物质的量和金属阳离子的物质的量的变化确定曲线对应的离子;
④结合转移电子的物质的量计算
解答 解:(1)氧离子核内有8个质子,核外有两个电子层,分别容纳2,8个电子,离子结构示意图: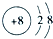 ,故答案为:
,故答案为: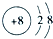
(2)Na2S为离子化合物,钠离子用离子符号表示,硫离子标出最外层电子,硫化钠的电子式为: ,
,
故答案为: ;
;
(3)电子层结构相同的离子,离子半径随着原子序数增大而减小;电子层不同的离子半径随电子层数的增多而增大,离子半径:S2->O2->Na+,故答案为:r(S2-)>r(O2-)>r(Na+);
(4)元素周期表中,同一周期元素从左到右元素的非金属性逐渐增强,则非金属性:Cl>S>Si,元素的非金属性越强,对应的最高价氧化物对应的水化合物酸性越强,故答案为:HClO4>H2SO4>H2SiO3;
(5)淡黄色固体A是Na2O2;液体X是H2O;气体Y是SO2;气体C则为O2;D溶液显酸性是NaHSO3.
①过氧化钠与水反应的要拆成离子,故答案为:2Na2O2+2H2O═4Na++OH-+O2↑;
②NaHSO3溶液呈酸性,NaHSO3溶液中存在亚硫酸氢根的水解与电离,水解导致其呈碱性,电离导致其呈酸性,据此分析:电离程度大于水解程度;故离子浓度大小为:c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>c(OH-),故答案为:c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>c(OH-);
(6))①据反应物和生成物可以确定该反应为2FeCl3+Cu═2FeCl2+CuCl2,所以X为FeCl3和FeCl2溶液,
故答案为:FeCl3和FeCl2;
②Cu做负极,石墨作正极,盐桥中阳离子向正极移动,则K+不断移向正极即进入X溶液中,
故答案为:K+;
③根据丙图可知溶液中有三种金属阳离子,而根据X的成分可知X中只有两种金属阳离子,说明在电解过程中还有Cu2+生成,它的物质的量从零逐渐增大,③为Cu2+,①表示的金属离子的物质的量正极减少,则为Fe3+,所以②为Fe2+,
故答案为:Fe2+;
④当电子转移为2mol时,溶液中有Fe3+ 2mol,Fe2+ 3mol,Cu2+为1mol,所以需要加入NaOH溶液14mol,所以NaOH溶液等体积为14mol÷5mol•L-1=2.8L,
故答案为:2.8.
点评 本题综合考查了物质结构与性质、电解质溶液、原电池和电解原理相关知识,综合性强,难度大,主要考查学生分析问题的能力,是高考的热点习题

 53天天练系列答案
53天天练系列答案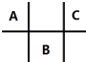 有四种短周期元素 A、B、C、D,其中 A、B、C 在周期表中所处的位置如图所示,且它们的质子数之和为 32.D 元素原子的最外层电子数为次外层电子数的2倍.则下列说法正确的是( )
有四种短周期元素 A、B、C、D,其中 A、B、C 在周期表中所处的位置如图所示,且它们的质子数之和为 32.D 元素原子的最外层电子数为次外层电子数的2倍.则下列说法正确的是( )| A. | 元素D形成的气态氢化物的空间结构一定是正四面体 | |
| B. | A、B 两种元素的气态氢化物均能不它们的最高价氧化物对应的水化物发生反应,且反应类型相同 | |
| C. | DB2、DC4中每个原子都满足8电子稳定结构 | |
| D. | 四种元素形成的气态氢化物中,C元素形成的氢化物的稳定性最高 |
 立方烷结构为立方体,其结构简式如图所示,立方烷的六氯代物有( )
立方烷结构为立方体,其结构简式如图所示,立方烷的六氯代物有( )| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
(1)用标准Na2CO3溶液滴定这种盐酸时,Na2CO3溶液应装在碱式滴定管中,若用甲基橙作指示剂,达到滴定终点时,溶液从红色变为橙色.
(2)现配制三种浓度的标准Na2CO3溶液,你认为最合适的是下列第③种(填序号).
①2.500mol•L-1 ②0.25mol•L-1 ③0.025mol•L-1
(3)若采用上述合适浓度的标准Na2CO3溶液滴定,用c(Na2CO3)表示,滴定时实验数据列表如下:
| 实验编号 | 待测盐酸体积(mL) | 滴入Na2CO3溶液体积(mL) |
| 1 | 20.00 | 18.80 |
| 2 | 20.00 | 16.95 |
| 3 | 20.00 | 17.05 |
(4)用A.偏高;B.偏低;C.无影响;D.无法判断,填写下列各项操作会给实验造成的误差.
①开始滴定时,滴定管尖端处有气泡,滴定完毕气泡排出A
②滴定前读数时仰视,滴定完毕读数时俯视B.
| A. | “丹砂(HgS)烧之成水银,积变又还成了丹砂”,该过程发生了氧化还原反应 | |
| B. | 大分子化合物油脂在人体内水解为氨基酸和甘油等小分子才能被吸收 | |
| C. | 利用植物油的氧化反应可以获得人造脂肪 | |
| D. | 干燥剂硅胶和硅橡胶的主要成分都是二氧化硅 |

(1)氮化硅(Si3N4)是一种新型陶瓷材料,它可由SiO2与过量焦炭在1300~1700°C的氮气流中反应制得:3SiO2(s)+6C(s)+2N2(g)?Si3N4(s)+6CO(g).△H=-1591.2kJ/mol,则该反应每转移1mole-,可放出的热量为132.6kJ.
(2)某研究小组现将三组CO(g)与H2O(g)的混合气体分别通入体积为2L的恒容密闭容器中,一定条件下发生反应:CO(g)+H2O(g)?CO2(g)+H2(g),得到如表数据:
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达平衡所需时间/mol | ||
| CO | H2O | CO | H2 | |||
| 1 | 650 | 2 | 4 | 0.5 | 1.5 | 5 |
| 2 | 900 | 1 | 2 | 0.5 | 0.5 | |
②下列能判断实验2已经达到平衡状态的是ad.
a.容器内CO、H2O、CO2、H2的浓度不再变化 b.容器内压强不再变化
c.混合气体的密度保持不变 d.v正(CO)=v逆(CO2)
e.容器中气体的平均相对分子质量不随时间而变化
③若实验2的容器是绝热的密闭容器,实验测得H2O(g)的转化率H2O%随时间变化的示意图如图1所示,b点v正>v逆(填“<”、“=”或“>”),t3~t4时刻,H2O(g)的转化率H2O%降低的原因是该反应达到平衡后,因反应为放热反应且反应容器为绝热容器,故容器内温度升高,反应逆向进行.
(3)利用CO与H2可直接合成甲醇,下图是由“甲醇-空气”形成的绿色燃料电池的工作原理示意图如图2,写出以石墨为电极的电池工作时负极的电极反应式CH3OH-6e-+H2O=CO2+6H+,利用该电池电解1L 0.5mol/L的CuSO4溶液,当消耗560mLO2(标准状况下)时,电解后溶液的pH=1(溶液电解前后体积的变化忽略不计).
| A. | F2 | B. | Br2 | C. | Cl2 | D. | N2 |

| A. | W点所示的溶液中:c(Na+)+c(H+)═2c(CO32-)+c(OH-)+c(Cl-) | |
| B. | pH=4的溶液中:c(H2CO3)+c(HCO32-)+c(CO32-)<0.1 mol•L-1 | |
| C. | pH=8的溶液中:c(H+)+c(H2CO3)+c(HCO3-)═c(OH-)+c(Cl-) | |
| D. | pH=11的溶液中:c(Na+)>c(Cl-)>c(CO32-)>c(HCO3- )>c(H2CO3) |
 、Cl-
、Cl- 、K+、Cl-、I-
、K+、Cl-、I- 、Cl-
、Cl-