题目内容
15.现有A、B、C、D四种气体,A是密度最小的气体,B在通常情况下呈黄绿色,把四种气体分别通入酸性硝酸银溶液中,通入B、D气体时立即出现白色沉淀,纯净的A可以在B中安静地燃烧,发出苍白色的火焰并生成D.把无色无刺激气味气体C通入澄清石灰水时变浑浊.(1)A、B、C、D的化学式分别为:AH2BCl2CCO2DHCl.
(2)写出下列各反应的化学方程式:A与B反应H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl
(3)上述实验中,C与澄清石灰水反应生成的沉淀质量为10g,则参加反应的气体在标准状况时的体积为2.24L.
分析 A是密度最小的气体,应为H2,B在通常情况下呈黄绿色,为Cl2,纯净的A可以在B中安静地燃烧,发出苍白色的火焰并生成D,则D为HCl;把无色无刺激气味气体C通入澄清石灰水时变浑浊,应为CO2,结合对应物质的性质解答该题.
解答 解:A是密度最小的气体,应为H2,B在通常情况下呈黄绿色,应为Cl2,纯净的A可以在B中安静地燃烧,发出苍白色的火焰并生成D,生成HCl,则D为HCl,把无色无刺激气味气体C通入澄清石灰水时变浑浊,应为CO2,
(1)由以上分析可知A为H2,B为Cl2,C为CO2,D为HCl,
故答案为:H2;Cl2;CO2;HCl;
(2)氢气在点燃条件下与氯气反应生成氯化氢,反应的方程式为:H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl,
故答案为:H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl;
(3)生成的10g沉淀为碳酸钙,其物质的量为:$\frac{10g}{100g/mol}$=0.1mol,根据C原子守恒可知消耗二氧化碳的物质的量为0.1mol,
标准状况下0.1mol二氧化碳的体积为:22.4L/mol×0.1mol=2.24L,
故答案为:2.24L.
点评 本题考查常见气体的检验方法,侧重于学生的分析能力和推断能力的考查,题目难度中等,明确常见气体的性质以及相关特征为解答该题的关键,注意熟练掌握相关气体的性质.

练习册系列答案
 走进文言文系列答案
走进文言文系列答案
相关题目
5.由两种气态烃组成的混合物,体积为10mL.与过量的氧气混合再充分燃烧,将生成物通过浓H2SO4气体体积减少25mL,再通过碱石灰气体体积又减少20mL(气体体积均为同温同压下).混合烃的组成可能为( )
| A. | C4H10和C2H4 | B. | C2H6和C2H4 | C. | CH4和C3H4 | D. | C2H4和C2H2 |
6.汽车剧烈碰撞时,安全气囊中发生反应:10NaN3+2KNO3=K2O+xNa2O+16N2↑,下列说法错误的是( )
| A. | x=5 | |
| B. | 每生成16 mol N2转移10 mol电子 | |
| C. | N2既是氧化产物又是还原产物 | |
| D. | 反应中氧化产物与还原产物的质量之比为1:15 |
3.科学家曾预言一种可用作炸药的物质,分子式为C(N3)4,其爆炸反应方程式为:C(N3)4→C+6N2↑,下列说法一定错误的是( )
| A. | 该物质为离子晶体 | |
| B. | 该物质可用通过C60吸附N2而制得 | |
| C. | C(N3)4中碳元素为正价 | |
| D. | 18g该物质完全分解可以产生13.44升(标准状况)氮气 |
20.用铜锌合金制成的假金元宝酷似黄金.下列不易区分真伪的方法是( )
| A. | 观察外观 | B. | 放入硝酸中 | C. | 放入盐酸中 | D. | 在空气中加热 |
5.下列化合物不能由单质直接合成的是( )
| A. | AlCl3 | B. | FeCl2 | C. | CuCl2 | D. | MgCl2 |
 .
.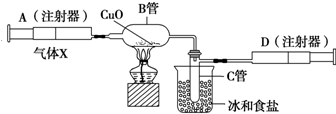 如图所示的实验装置可用来测定含两种元素的某种气体X的分子式.在注射器A中装有240mL气体X并慢慢通过不含空气并装有红热的氧化铜的玻璃管B,使之完全反应,得到以下实验结果:实验前B管重20.32g,实验后B管重20.00g,B管中的黑色粉末变成红色粉末.在C管中收集到的无色液体是水;在注射器D中收集到的气体是氮气.试回答下列问题:
如图所示的实验装置可用来测定含两种元素的某种气体X的分子式.在注射器A中装有240mL气体X并慢慢通过不含空气并装有红热的氧化铜的玻璃管B,使之完全反应,得到以下实验结果:实验前B管重20.32g,实验后B管重20.00g,B管中的黑色粉末变成红色粉末.在C管中收集到的无色液体是水;在注射器D中收集到的气体是氮气.试回答下列问题: