题目内容
13.以锌锰废电池中的碳包为原料回收MnO2的过程中涉及如下反应:①MnO2(s)+C(s)═MnO(s)+CO(g)△H1=+24.4kJ•mol-1
②MnO2(s)+CO(g)═MnO(s)+CO2(g)△H2=-148.1kJ•mol-1
③2MnO2(s)+C(s)═2MnO(s)+CO2(g)△H3
则下列判断正确的是( )
| A. | 碱性锌锰干电池属于二次电池 | B. | △H3=△H1+△H2 | ||
| C. | 反应①的活化能为24.4 kJ•mol-1 | D. | △H1<△H3 |
分析 A、碱性锌锰干电池属于一次电池;
B、由反应①MnO2(s)+C(s)═MnO(s)+CO(g)△H1=+24.4kJ•mol-1
②MnO2(s)+CO(g)═MnO(s)+CO2(g)△H2=-148.1kJ•mol-1,根据盖斯定律可知:△H3=△H1+△H2;
C、由反应MnO2(s)+C(s)═MnO(s)+CO(g)△H1=+24.4kJ•mol-1可知,24.4 kJ•mol-1是反应热;
D、由B选项可知:△H3=△H1+△H2,所以△H3-△H1=△H2,而△H2=-148.1kJ•mol-<0,所以△H3-△H1<0,由此分析解答.
解答 解:A、碱性锌锰干电池属于一次电池,而不是二次电池,故A错误;
B、由反应①MnO2(s)+C(s)═MnO(s)+CO(g)△H1=+24.4kJ•mol-1;②MnO2(s)+CO(g)═MnO(s)+CO2(g)△H2=-148.1kJ•mol-1,根据盖斯定律可知:△H3=△H1+△H2,故B正确;
C、由反应MnO2(s)+C(s)═MnO(s)+CO(g)△H1=+24.4kJ•mol-1可知,24.4 kJ•mol-1是反应热,而不是活化能,故C错误;
D、由B选项可知:△H3=△H1+△H2,所以△H3-△H1=△H2,而△H2=-148.1kJ•mol-<0,所以△H3-△H1<0,则△H1>△H3,故D错误;
故选B.
点评 本题考查原电池的分类、盖斯定律的应用和计算,涉及到电池的分类、反应热大小的比较,题目难度不大,建议把相关基础知识掌握好.

练习册系列答案
相关题目
3.下列有关“水”的说法中正确的是( )
| A. | 双氧水被称为绿色氧化剂,是因为其还原产物为O2,对环境无污染 | |
| B. | 王水是浓盐酸和浓硝酸按体积比1:3配成的混合物,可溶解Au、Pt | |
| C. | 氨水能导电,说明氨气是电解质 | |
| D. | 往新制备的氯水中和SO2的水溶液中分别滴入石蕊试液时的现象不同 |
1.分析下列反应在任何温度下均能自发进行的是( )
| A. | 2N2(g)+O2(g)═2N2O(g)△H=+163 kJ•mol-1 | |
| B. | Ag(s)+$\frac{1}{2}$Cl2(g)═AgCl(s)△H=-127 kJ•mol-1 | |
| C. | HgO(s)═Hg(l)+$\frac{1}{2}$O2(g)△H=+91 kJ•mol-1 | |
| D. | H2O2(l)═$\frac{1}{2}$O2(g)+H2O(l)△H=-98 kJ•mol-1 |
18.某种兴奋剂的结构简式如图所示,有关该物质的说法错误的是( )
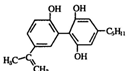

| A. | 该有机物不仅能使溴水、酸性 KMnO4 溶液褪色,也能与FeCl3溶液发生显色反应 | |
| B. | 一定条件下该有机物能发生加成反应、氧化反应、取代反应,也能发生聚合反应 | |
| C. | 该有机物中可能存在手性碳原子 | |
| D. | 该有机物显弱酸性,能与 NaOH 溶液、NaHCO3 溶液发生反应 |
5.下列各化合物的命名正确的是( )
| A. | CH2=CH-CH=CH2 1,3-二丁烯 | |
| B. | CH3COOCH2CH2OOCCH3 乙二酸二乙酯 | |
| C. | CH3CH2CH(OH)CH3 3-丁醇 | |
| D. | 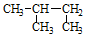 2-甲基丁烷 2-甲基丁烷 |
3.下列实验中,对应的现象以及结论都正确且两者具有因果关系的是( )
| 选项 | 实验 | 现象 | 结论 |
| A | 将滴有酚酞的0.1mol•L-1氨水系稀释成0.01mol•L-1 | 溶液颜色变浅 | 稀释后NH3•H2O的电离程度减小 |
| B | 将铜粉加入1.0mol•L-1Fe2(SO4)3溶液中 | 溶液变蓝、有黑色固体出现 | 金属铁比铜活泼 |
| C | 用溴乙烷与NaOH乙醇溶液共热产生的气体通入酸性KMnO4溶液中 | 溶液褪色 | 产生的气体为乙烯 |
| D | 向1mL0.1mol•L-1 MgSO4溶液滴入2滴等浓度的NaOH溶液,片刻后再滴加2滴0.1mol•L-1 CuSO4溶液 | 先有白色沉淀生成,后变为蓝色沉淀 | Cu(OH)2的溶度积常数比Mg(OH)2的小 |
| A. | A | B. | B | C. | C | D. | D |