题目内容
有甲、乙两位同学分别做碳酸钠溶液和盐酸反应的实验.甲同学将80ml 1mol?L-1的碳酸钠溶液逐滴加入到100ml 1mol?L-1的盐酸中去;乙同学则将100ml 1mol?L-1的盐酸逐滴加入到80ml 1mol?L-1的碳酸钠溶液中去,甲、乙两位同学产生的CO2气体的体积比为( )
| A、1:1 | B、4:5 |
| C、5:2 | D、5:4 |
考点:化学方程式的有关计算
专题:计算题
分析:甲同学实验,发生反应:Na2CO3+2HCl=2NaCl+CO2↑+H2O;乙同学实验,首先发生反应:Na2CO3+HCl=NaHCO3+NaCl,然后发生反应:NaHCO3+HCl=NaCl+CO2↑+H2O,结合方程式计算生成二氧化碳体积,据此解答.
解答:
解:碳酸钠的物质的量=0.08L×1mol/L=0.08mol,HCl的物质的量=0.1L×1mol/L=0.1mol,
甲同学实验,发生反应:
Na2CO3+2HCl=2NaCl+CO2↑+H2O
0.08mol 0.16mol
故HCl不足,由方程式可知,0.1molHCl反应生成二氧化碳为0.1mol×
=0.05mol,
乙同学实验,首先发生:
Na2CO3+HCl=NaHCO3+NaCl
0.08mol 0.08mol 0.08mol
剩余HCl为0.1mol-0.08mol=0.02mol,
然后发生反应:
NaHCO3+HCl=NaCl+CO2↑+H2O,
0.08mol 0.08mol
故盐酸不足,由方程式可知,0.02molHCl反应生成二氧化碳为0.02mol;
故甲、乙两位同学产生的CO2气体的体积比为0.05mol:0.02mol=5:2
故选C.
甲同学实验,发生反应:
Na2CO3+2HCl=2NaCl+CO2↑+H2O
0.08mol 0.16mol
故HCl不足,由方程式可知,0.1molHCl反应生成二氧化碳为0.1mol×
| 1 |
| 2 |
乙同学实验,首先发生:
Na2CO3+HCl=NaHCO3+NaCl
0.08mol 0.08mol 0.08mol
剩余HCl为0.1mol-0.08mol=0.02mol,
然后发生反应:
NaHCO3+HCl=NaCl+CO2↑+H2O,
0.08mol 0.08mol
故盐酸不足,由方程式可知,0.02molHCl反应生成二氧化碳为0.02mol;
故甲、乙两位同学产生的CO2气体的体积比为0.05mol:0.02mol=5:2
故选C.
点评:本题考查化学方程式的有关计算,关键是明确滴加顺序不同发生的不同的反应,难度不大.

练习册系列答案
相关题目
若ag某气体中含有的分子数为b,则cg该气体的物质的量为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
用如图实验装置进行相应实验,能达到实验目的是( )

| A、用图1所示装置分离沸点相差较大的互溶液体混合物 |
| B、用图2所示装置蒸干FeCl2饱和溶液制备FeCl2晶体 |
| C、用图3所示装置稀释浓硫酸 |
| D、用图4所示装置分离CCl4萃取碘水后已分层的有机层和水层 |
下列关于图的实验装置说法正确的是( )
A、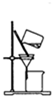 该图装置可以提纯精制氢氧化铁胶体 |
B、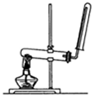 该图装置可以用来制备和收集氨气和氧气 |
C、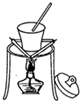 该图可以从食盐水中得到食盐晶体 |
D、 该图试管中放新制FeSO4溶液,从滴管中滴加NaOH溶液,易于观察到Fe(OH)2颜色 |
设NA为阿伏加德罗常数的值,下列有关叙述不正确的是( )
| A、1 mol碳正离子(CH+3)所含的电子总数为8NA | ||
| B、1 mol甲基(-CH3)所含的电子总数为9NA | ||
| C、0.5 摩1,3-丁二烯分子中含有C=C双键数为 NA | ||
D、标准状况下,1L庚烷完全燃烧所生成的气态产物的分子数为
|
下列表示对应化学反应的离子方程式正确的是( )
A、向氯化铝溶液通入过量的氨气:Al3++4OH-═
| ||||
B、MnO2与浓盐酸反应制Cl2:MnO2+4HCl
| ||||
| C、FeCl3溶液用于蚀刻印刷电路:Cu+2Fe3+=Cu2++2Fe2+ | ||||
| D、在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3ClO-+Fe(OH)3=FeO42-+3Cl-+H2O+4H+ |
1.2mol Cl2与元素A单质完全反应生成0.80mol AClx,则x值为( )
| A、1 | B、2 | C、3 | D、4 |
某气态烃在密闭容器内与氧气混合完全燃烧,如果燃烧前后容器内(温度高于1000C)压强保持不变,该烃可能是( )
| A、C2H6 |
| B、C2H4 |
| C、C3H8 |
| D、C3H6 |
鉴别晶体与非晶体最可靠的科学方法是( )
| A、红外光谱 | B、X射线衍射实验 |
| C、质谱 | D、原子光谱 |