题目内容
NA表示阿佛加德罗常数,下列说法正确的是( )
| A、60克SiO2含有2NA个Si-O共价键 |
| B、实验室中用含4molHCl的浓盐酸跟足量MnO2加热反应可制得Cl2的分子数为NA |
| C、1L 0.2mol?L-1Al2(SO4)3溶液中的离子总数为NA |
| D、标准状况下,22.4LCO2约含有 3NA个原子 |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、依据n=
计算物质的量,结合二氧化硅结构中共价键计算;
B、浓盐酸和二氧化锰反应随浓度减小后,不能继续反应生成氯气;
C、铝离子水解阳离子数增多;
D、依据n=
计算物质的量结合分子式计算原子数.
| m |
| M |
B、浓盐酸和二氧化锰反应随浓度减小后,不能继续反应生成氯气;
C、铝离子水解阳离子数增多;
D、依据n=
| V |
| Vm |
解答:
解:A、依据n=
计算物质的量=
=1mol,结合二氧化硅结构中共价键计算含有Si-O共价键4NA个,故A错误;
B、浓盐酸和二氧化锰反应随浓度减小后,不能继续反应生成氯气,4molHCl的浓盐酸跟足量MnO2加热反应可制得Cl2的分子数小于NA,故B错误;
C、铝离子水解阳离子数增多,1L 0.2mol?L-1Al2(SO4)3溶液中的离子总数大于NA,故C错误;
D、依据n=
计算物质的量=
=1mol,结合分子式计算原子数为3NA个原子,故D正确;
故选D.
| m |
| M |
| 60g |
| 60g/mol |
B、浓盐酸和二氧化锰反应随浓度减小后,不能继续反应生成氯气,4molHCl的浓盐酸跟足量MnO2加热反应可制得Cl2的分子数小于NA,故B错误;
C、铝离子水解阳离子数增多,1L 0.2mol?L-1Al2(SO4)3溶液中的离子总数大于NA,故C错误;
D、依据n=
| V |
| Vm |
| 22.4L |
| 22.4L/mol |
故选D.
点评:本题考查了阿伏伽德罗常数的分析应用,主要是气体摩尔体积条件分析,反应过程理解应用,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
NA为阿伏加德罗常数的值,下列说法正确的是( )
| A、25℃,pH=13的NaOH溶液中含有OH-的数目为0.1NA |
| B、在密闭容器中加入1mol N2和3mol H2,一定条件下充反应生成NH3分子数小于2NA |
| C、将0.1mol FeCl3溶于1L水中,所得溶液含有0.1NA个Fe3+ |
| D、1L 1mol/L的KF溶液中含有F-的数目为NA |
设阿伏加德罗常数为NA,下列说法正确的是( )
| A、2 L 0.5 mol?L-1硫酸钾溶液中阴离子所带电荷数为NA |
| B、常温常压下,14g氮气中含有 NA个原子 |
| C、1mol/LNaCl溶液中含有NA个氯离子 |
| D、等质量的丙烯和乙烯气体中氢原子的个数均为6NA |
下列物质中,在标准状况下体积最大的是( )
| A、48g O2 |
| B、71g Cl2 |
| C、28g N2 |
| D、1000g H2O |
下列各种描述中,正确的是( )
| A、氯水具有杀菌消毒作用,其中起作用的物质是氯气 |
| B、加碘食盐中所加的“碘”一般是碘化钾 |
| C、区别氯化铁溶液和氢氧化铁胶体可以用丁达尔效应 |
| D、用干燥的有色布条可以检验氯化氢气体中是否混有氯气 |
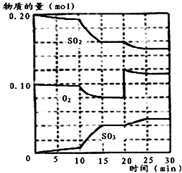 已知一定条件下在1L的密封容器中,发生如下反应:2SO2(g)+O2(g)?2SO3(g),△H<0,反应过程中SO2、O2、SO3物质的量变化如图,请根据图示回答下列问题:
已知一定条件下在1L的密封容器中,发生如下反应:2SO2(g)+O2(g)?2SO3(g),△H<0,反应过程中SO2、O2、SO3物质的量变化如图,请根据图示回答下列问题: