题目内容
称取3.07g化合物D溶解于过量NaOH水溶液中,在所得溶液加硝酸中和至pH=7,并加入过量的硝酸钙;得到白色沉淀过滤、干燥,称重,重量为3.1g.向剩余溶液中加入过量硝酸银,又生成8.61g白色沉淀.
(1)判断化合物D,并写出所有反应过程的方程式;
(2)写出化合物D与水反应的方程式.
(1)判断化合物D,并写出所有反应过程的方程式;
(2)写出化合物D与水反应的方程式.
考点:化学方程式的有关计算
专题:计算题
分析:向剩余溶液中加入过量硝酸银,又生成8.61g白色沉淀,则该沉淀为氯化银,氯化银的物质的量为
=0.06mol,氯离子的质量为:0.06mol×35.5g/mol=2.13g,能和硝酸钙生成沉淀,则阴离子可能为磷酸根离子,3.1g磷酸钙的物质的量为
=0.01mol,含P0.02mol,质量为:0.02mol×31g/mol=0.62g,P和Cl的物质的量之比为1:3,根据生成磷酸钙,可知磷的化合价为+5,氯的为-1,故还应含有氧原子,质量为3.07g-2.13g-0.62g=0.32g,物质的量为
=0.02mol,P、O、Cl个数比为1:1:3,故D为POCl3,D和氢氧化钠反应生成磷酸钠和氯化钠,磷酸钠和硝酸钙反应生成磷酸钙和硝酸钠,氯化钠和硝酸银反应生成氯化银和硝酸钠,写出方程式即可.
| 8.61g |
| 143.5g/mol |
| 3.1g |
| 310g/mol |
| 0.32g |
| 16g/mol |
解答:
解:(1)向剩余溶液中加入过量硝酸银,又生成8.61g白色沉淀,则该沉淀为氯化银,氯化银的物质的量为
=0.06mol,氯离子的质量为:0.06mol×35.5g/mol=2.13g,能和硝酸钙生成沉淀,则阴离子可能为磷酸根离子,3.1g磷酸钙的物质的量为
=0.01mol,含P0.02mol,质量为:0.02mol×31g/mol=0.62g,P和Cl的物质的量之比为1:3,根据生成磷酸钙,可知磷的化合价为+5,氯的为-1,故还应含有氧原子,质量为:3.07g-2.13g-0.62g=0.32g,物质的量为:
=0.02mol,P、O、Cl个数比为:1:1:3,故D为POCl3,D和氢氧化钠反应生成磷酸钠和氯化钠,反应方程式为:POCl3+6NaOH=Na3PO4+3NaCl+3H2O,磷酸钠和硝酸钙反应生成磷酸钙和硝酸钠,反应方程式为:2Na3PO4+3Ca(NO3)2=Ca3(PO4)2↓+6NaNO3,氯化钠和硝酸银反应生成氯化银和硝酸钠,方程式为:
AgNO3+NaCl=AgCl↓+NaNO3,
答:D的化学式为POCl3,POCl3+6NaOH=Na3PO4+3NaCl+3H2O,2Na3PO4+3Ca(NO3)2=Ca3(PO4)2↓+6NaNO3,AgNO3+NaCl=AgCl↓+NaNO3;
(2)POCl3和氢氧化钠反应生成磷酸钠和氯化钠,则三氯氧磷和水反应生成磷酸和盐酸,反应方程式为3H2O+POCl3=H3PO4+3HCl,
答:化合物D与水反应的方程式为3H2O+POCl3=H3PO4+3HCl.
| 8.61g |
| 143.5g/mol |
| 3.1g |
| 310g/mol |
| 0.32g |
| 16g/mol |
AgNO3+NaCl=AgCl↓+NaNO3,
答:D的化学式为POCl3,POCl3+6NaOH=Na3PO4+3NaCl+3H2O,2Na3PO4+3Ca(NO3)2=Ca3(PO4)2↓+6NaNO3,AgNO3+NaCl=AgCl↓+NaNO3;
(2)POCl3和氢氧化钠反应生成磷酸钠和氯化钠,则三氯氧磷和水反应生成磷酸和盐酸,反应方程式为3H2O+POCl3=H3PO4+3HCl,
答:化合物D与水反应的方程式为3H2O+POCl3=H3PO4+3HCl.
点评:本题考查了物质的推断,难度较大,推测含氧是解题的关键,注意化合价守恒的应用.

练习册系列答案
相关题目
下列说法正确的是( )
| A、氮原子的质量就是氮的相对原子质量 |
| B、氢氧化钠的摩尔质量是40 g |
| C、1 mol H2SO4中含有1 mol H2 |
| D、氩气的摩尔质量在数值上等于它的相对原子质量 |
在一容积固定的密闭容器中进行反应:2SO2(g)+O2(g)??2SO3(g).已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2mol?L-1、0.1mol?L-1、0.2mol?L-1.当反应达到平衡时,各物质的浓度可能存在的数据是( )
| A、SO2为0.4 mol?L-1,O2为0.2 mol?L-1 |
| B、SO2为0.25 mol?L-1 |
| C、SO2和SO3均为0.15 mol?L-1 |
| D、SO2为0.4 mol?L-1 |
浓度均为0.1mol.L-1的Na2CO3和盐酸各0.5L,有甲乙两位同学进行实验,甲向Na2CO3溶液中滴加盐酸至完全反应乙向盐酸中滴加Na2CO3至完全反应.两位同学在实验过程中产生的CO2气体比较结果正确的是( )
| A、甲>乙 | B、甲<乙 |
| C、甲=乙 | D、无法确定 |
农药波尔多液不能用铁制容器盛放,是因为铁能与该农药中的硫酸铜起反应.该反应中,铁是( )
| A、氧化剂 | B、被还原 |
| C、还原剂 | D、氧化产物 |
将20.8g两种金属的混合物投入足量的盐酸中,反应完全后得到标准状况下氢气11.2L,该混合物的组成可能是( )
| A、铜和锌 | B、镁和铜 |
| C、铝和镁 | D、锌和铁 |
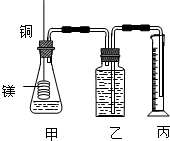 某研究性学习小组为证明在同温同压下,相同浓度相同体积的不同强度的一元酸与足量镁带反应时,生成氢气的体积相同而反应速率不同,同时测定实验室条件下的气体摩尔体积设计的简易实验装置图.该实验的主要操作步骤如下:
某研究性学习小组为证明在同温同压下,相同浓度相同体积的不同强度的一元酸与足量镁带反应时,生成氢气的体积相同而反应速率不同,同时测定实验室条件下的气体摩尔体积设计的简易实验装置图.该实验的主要操作步骤如下: