题目内容
7.下列各表述与示意图一致的是( )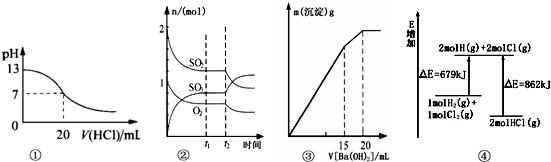
| A. | 图①表示25℃时,用0.1 mol/L盐酸滴定20 mL 0.1 mol/L NaOH溶液,溶液的pH随加入酸体积的变化得到的滴定曲线 | |
| B. | 图②表示一定条件下进行的反应2SO2(g)+O2(g)?2SO3(g)△H<0各成分的物质的量变化,t2时刻改变的条件可能是降低温度或缩小容器体积 | |
| C. | 图③表示某明矾溶液中加入Ba(OH)2溶液,沉淀的质量与加入Ba(OH)2溶液体积的关系,在加入20 mL Ba(OH)2溶液时铝离子恰好沉淀完全 | |
| D. | 图④表示化学反应H2(g)+C12(g)═2HCl(g)的能量变化,则该反应的反应热△H=﹢183 kJ/mol |
分析 A.酸碱中和在接近终点时,pH会发生突变,曲线的斜率应该很大,图象曲线变化与实际不相符;
B.根据图②曲线变化可知,t2时刻后二氧化硫和氧气的物质的量减小,而三氧化硫的物质的量增大,说明平衡正向移动,结合反应为气体体积缩小的反应及平衡移动原理分析;
C.向明矾溶液中加入Ba(OH)2溶液,开始阶段生成硫酸钡和氢氧化铝沉淀,随后继续生成硫酸钡沉淀,而氢氧化铝沉淀溶解,最后沉淀完全为硫酸钡,沉淀质量达到最大时氢氧化铝完全溶解;
D.反应H2(g)+C12(g)═2HCl(g)为放热反应,该反应的反应热△H应该为负值.
解答 解:A.0.1mol•L-1NaOH溶液的pH为13,用0.1mol•L-1盐酸滴定恰好中和时pH为7,因浓度相同,则体积相同,但酸碱中和在接近终点时,pH会发生突变,曲线的斜率会很大,图象曲线变化与实际不相符,故A错误;
B.根据图②分析,t2时刻后二氧化硫和氧气的物质的量减小,而三氧化硫的物质的量增大,说明平衡正向移动,结合反应的特点及平衡移动原理分析,t2时刻改变的条件可能是降低温度或缩小容器体积,故B正确;
C.向明矾溶液中加入Ba(OH)2溶液,开始阶段生成硫酸钡和氢氧化铝沉淀,随后形成硫酸钡沉淀,而氢氧化铝沉淀溶解,最后沉淀为硫酸钡,由图象可知,在加入20 mL Ba(OH)2溶液时铝离子恰好转化为偏铝酸根,故C错误;
D.根据图④分析,反应H2(g)+C12(g)═2HCl(g)为放热反应,则该反应的反应热△H=-183 kJ/mol,故D错误;
故选B.
点评 本题考查较为综合,涉及中和滴定、热化学方程式书写、化学平衡及其影响、离子反应的应用等知识,题目难度中等,注意掌握反应热与焓变的关系,C为易错点,明确发生反应原理为解答关键,试题培养了学生的分析能力及灵活应用能力.

 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案| A. | 在氧化还原反应中,还原剂一定是失去电子的反应物 | |
| B. | 在氧化还原反应中,非金属单质一定是氧化剂 | |
| C. | 某元素从化合态转变为游离态时,该元素一定被还原 | |
| D. | 金属阳离子被还原不一定得到金属单质 |
| 选项 | 类别 | 物质 |
| A | 碱性氧化物 | Na2O2 CuO MgO |
| B | 难溶性物质 | Ba(OH)2 MgSO4 Na2SiO3 |
| C | 弱酸 | H2S H2SO4 CH3COOH |
| D | 强电解质 | AgCl MgSO4 CaCO3 |
| A. | A | B. | B | C. | C | D. | D |
| A. | NO和O2 | B. | SO2和O2 | C. | NO2和NO | D. | NH3和O2 |
(1)弱酸在水溶液中存在电离平衡,部分0.1mol•L-1弱酸的电离平衡常数如下表:
| 弱酸 | 电离平衡常数(25℃) |
| HClO | K=2.98×10-8 |
| H2CO3 | K1=4.3×10-7 K2=5.6×10-11 |
| H2SO3 | K1=1.54×10-2 K2=1.02×10-7 |
②下列离子方程式和有关说法错误的是ac.
a.少量的CO2通入次氯酸钠溶液中:2ClO-+H2O+CO2═2HClO+CO32-
b.少量的SO2通入碳酸钠溶液中:SO2+H2O+2CO32-═2HCO3-+SO32-
c.相同温度时,等物质的量浓度的三种弱酸与足量NaOH溶液完全中和消耗NaOH的体积为V(H2CO3)>V(H2SO3)>V(HClO)
d.相同温度时,等pH三种盐溶液的物质的量浓度关系:c(Na2CO3)<c(NaClO)<c(Na2SO3)
③亚硒酸(H2SeO3)也是一种二元弱酸,有较强的氧化性.往亚硒酸溶液中不断通入SO2会产生红褐色单质,写出该反应的化学方程式:H2SeO3+2SO2+H2O=Se↓+2H2SO4.
(2)工业废水中常含有一定量的Cr2O72-和CrO42-,它们对人类及生态系统会产生很大损害,必须进行处理后方可排放.
①在废水中存在平衡:2CrO42-(黄色)+2H+?Cr2O72-(橙色)+H2O.若改变条件使上述平衡向逆反应方向移动,则下列说法正确的是ad.
a.平衡常数K值可以不改变
b.达到新平衡CrO42-的消耗速率等于Cr2O72-的消耗速率
c.达到新平衡后,溶液pH一定增大
d.再达平衡前逆反应速率一定大于正反应速率
②Cr2O72-和CrO42-最终生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s)?Cr3+(aq)+3OH-(aq),常温下Cr(OH)3的Ksp=10-32,当c(Cr3+)降至10-3 mol•L-1,溶液的pH调至4时,没有(填“有”或“没有”)沉淀产生.
(3)已知:①2CH3OH(g)?CH3OCH3(g)+H2O(g)
②CO(g)+2H2(g)?CH3OH(g)
③CO(g)+H2O(g) CO2(g)+H2(g)
某温度下三个反应的平衡常数的值依次为K1、K2、K3,则该温度下反应3CO(g)+3H2(g)?CH3OCH3(g)+CO2(g)的化学平衡常数K=K1K22K3(用含K1、K2、K3的代数式表示).向某固定体积的密闭容器中加入3mol CO和3mol H2,充分反应后恢复至原温度,测定容器的压强为反应前的$\frac{1}{2}$,则CO的转化率为75%.
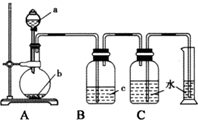 如图是制取、净化并测量生成气体体积的装置示意图.利用如图装置进行表所列实验,能达到实验目的是 ( )
如图是制取、净化并测量生成气体体积的装置示意图.利用如图装置进行表所列实验,能达到实验目的是 ( )| 选项 | a(液体) | b(固体) | c(液体) |
| A | 稀盐酸 | 锌粒 | 浓硫酸 |
| B | 浓氨水 | 生石灰 | 浓硫酸 |
| C | 饱和食盐水 | 电石 | 硫酸铜溶液 |
| D | 浓硫酸 | Cu片 | 氢氧化钠溶液 |
| A. | A | B. | B | C. | C | D. | D |
 (1)写出工业上分别以①CH2=CH2为原料和②C6H12O6为原料制取乙醇的化学方程式:①CH2=CH2+H2O$→_{高温高压}^{催化剂}$CH3CH2OH②C6H12O6$\stackrel{催化剂}{→}$2CO2↑+2CH3CH2OH
(1)写出工业上分别以①CH2=CH2为原料和②C6H12O6为原料制取乙醇的化学方程式:①CH2=CH2+H2O$→_{高温高压}^{催化剂}$CH3CH2OH②C6H12O6$\stackrel{催化剂}{→}$2CO2↑+2CH3CH2OH