题目内容
 卤素单质的性质活泼,卤素的化合物应用广泛,研究卤素单质及其化合物具有重要意义.
卤素单质的性质活泼,卤素的化合物应用广泛,研究卤素单质及其化合物具有重要意义.(1)在光照条件下,氯气和氢气反应过程如下:
①Cl2→Cl+Cl ②Cl+H2→HCl+H ③H+Cl→HCl+Cl氯元素的原子结构示意图为
(2)二氧化氯(ClO2)是一种广泛用于水处理消毒剂,与Cl2相比,ClO2不但具有更显著的杀菌能力,而且不会产生对人体有害的有机氯化物.制备Cl02的方法有以下两种:
2NaClO3+4HCl═2ClO2↑+Cl2↑+2NaCl+2H2O…①
2NaClO2+H2O2+H2SO4═2ClO2↑+O2↑+Na2SO4+2H2O…②
你认为哪种方法最佳
(3)工业上用电解饱和食盐水的方法制取烧碱和氯气,请写出反应的离子方程式
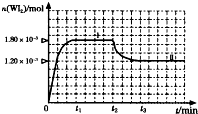
(4)碘钨灯具有比白炽灯寿命长且环保节能的特点.一定温度下,灯泡内封存的少量碘与使用过程中沉积在管壁上的钨可以发生反应:W(s)+I2(g)?WI2(g).为模拟上述反应,准确称取0.508g碘、0.736g金属钨置于50.0mL的密闭容器中,加热使其反应.如图是WI2(g)的物质的量随时间变化关系图象,其中曲线I(0~t2时间段)的反应温度为T1,曲线Ⅱ(从t2开始)的反应温度为T2,且T2>T1.则:①该反应的△H
②从反应开始到t1时间内的平均反应速率v(I2)=
③下列说法中不正确的是
A.该反应的平衡常数表达式是K=
| c(WI2) |
| c(W)?c(I2) |
B.灯丝附近温度越高,灯丝附近区域WI2越易变为W而重新沉积到灯丝上
C.利用该反应原理可以提纯钨
(5)25℃时,向5mL含有KCI和KI浓度均为0.1mol/L的混合液中,滴加6mL 0.lmol/L的AgNO3溶液,先生成的沉淀是
(6)Mg常用作提纯Ti的试剂,已知:
①Mg(s)+Cl2(g)═MgCl2(s)△H=-64kJ/mol
②Ti(s)+2Cl2(g)═TiCl4(l)△H=-770kJ/mol
请写出Mg与液态TiCl4反应提纯钛的热化学方程式
考点:物质的量或浓度随时间的变化曲线,氯碱工业,热化学方程式,化学平衡的影响因素,难溶电解质的溶解平衡及沉淀转化的本质,氯、溴、碘及其化合物的综合应用
专题:化学平衡专题,元素及其化合物
分析:(1)Cl原子核外有3个电子层,最外层电子数为7;
(2)制备物质,应尽可能考虑原料的利用率以及环境污染等问题;
(3)电解饱和食盐水生成氯气、氢气和氢氧化钠;
(4)①由图象可知,升高温度,WI2的物质的量减小,说明平衡逆向移动;
②根据公式v=
来计算反应速率;
③化学平衡常数=
;
(5)越是难溶的沉淀越容易生成,结合物质的量的多少以及反应的程度比较;
(6)根据盖斯定律来计算反应的焓变,以此书写热化学方程式.
(2)制备物质,应尽可能考虑原料的利用率以及环境污染等问题;
(3)电解饱和食盐水生成氯气、氢气和氢氧化钠;
(4)①由图象可知,升高温度,WI2的物质的量减小,说明平衡逆向移动;
②根据公式v=
| △c |
| △t |
③化学平衡常数=
| 生成物浓度系数次方的乘积 |
| 反应物浓度系数次方的乘积 |
(5)越是难溶的沉淀越容易生成,结合物质的量的多少以及反应的程度比较;
(6)根据盖斯定律来计算反应的焓变,以此书写热化学方程式.
解答:
解:(1)Cl原子核外有3个电子层,最外层电子数为7,原子结构示意图为: ,故答案为:
,故答案为: ;
;
(2)根据反应方程式,方法①制备ClO2的产物氯气有毒,对空气会造成污染,而方法②生成的氧气是不会造成污染的,
故答案为:②;ClO2中混有O2,不会产生对人体有害的物质;
(3)电解饱和食盐水的原理方程式为:2C1-+2H2O
Cl2↑+H2↑+2OH-,故答案为:2C1-+2H2O
Cl2↑+H2↑+2OH-;
(4)①根据图示,温度越高,WI2(g)的物质的量反而越小,即平衡向左进行,而升高温度,化学平衡向着吸热方向进行,所以逆向是吸热方向,正向是放热的,故△H小于0,故答案为:<;
②从反应开始到t1时间内,结合图象,生成WI2(g)的物质的量为1.8×10-3mol,所以碘单质的物质的量减少1.8×10-3mol,
v=
=
=
mol?L-1?min-1,
故答案为:
mol?L-1?min-1;
③A.化学平衡常数=
,但是固体单质W不列入表达式中,故A错误;
B.灯丝附近温度越高,化学平衡越向着吸热方向即逆向进行,灯丝附近区域WI2越易变为W而重新沉积到灯丝上,故B正确;
C.通过碘与钨的反应可分离、提纯钨,然后再加高温度下,通过碘易升华的性质分离碘和钨,故C正确;
故答案为:A;
(5)碘化银的溶度积最小,越容易生成,溶液混合反应之后,溶液的组成为:含有0.001mol的钾离子,0.0006mol的硝酸根离子,以及0.0004mol的氯离子,碘化银沉淀生成,碘离子全沉淀,氯化银沉淀也产生,均为0.0005mol但是AgCl的电离程度大,故答案为:AgI; c(K+)>c(NO-3)>c(Cl-)>c(Ag+)>c(I-);
(6)根据盖斯定律来计算反应的焓变,目标反应=①×2-②,即热化学方程式为:2Mg(s)+TiCl4(1)=2MgCl2(s)+Ti(s)△H=-512kJ?mol-1,
故答案为:2Mg(s)+TiCl4(1)=2MgCl2(s)+Ti(s)△H=-512kJ?mol-1.
 ,故答案为:
,故答案为: ;
;(2)根据反应方程式,方法①制备ClO2的产物氯气有毒,对空气会造成污染,而方法②生成的氧气是不会造成污染的,
故答案为:②;ClO2中混有O2,不会产生对人体有害的物质;
(3)电解饱和食盐水的原理方程式为:2C1-+2H2O
| ||
| ||
(4)①根据图示,温度越高,WI2(g)的物质的量反而越小,即平衡向左进行,而升高温度,化学平衡向着吸热方向进行,所以逆向是吸热方向,正向是放热的,故△H小于0,故答案为:<;
②从反应开始到t1时间内,结合图象,生成WI2(g)的物质的量为1.8×10-3mol,所以碘单质的物质的量减少1.8×10-3mol,
v=
| △c |
| △t |
| ||
| t1min |
| 0.036 |
| t1 |
故答案为:
| 0.036 |
| t1 |
③A.化学平衡常数=
| 生成物浓度系数次方的乘积 |
| 反应物浓度系数次方的乘积 |
B.灯丝附近温度越高,化学平衡越向着吸热方向即逆向进行,灯丝附近区域WI2越易变为W而重新沉积到灯丝上,故B正确;
C.通过碘与钨的反应可分离、提纯钨,然后再加高温度下,通过碘易升华的性质分离碘和钨,故C正确;
故答案为:A;
(5)碘化银的溶度积最小,越容易生成,溶液混合反应之后,溶液的组成为:含有0.001mol的钾离子,0.0006mol的硝酸根离子,以及0.0004mol的氯离子,碘化银沉淀生成,碘离子全沉淀,氯化银沉淀也产生,均为0.0005mol但是AgCl的电离程度大,故答案为:AgI; c(K+)>c(NO-3)>c(Cl-)>c(Ag+)>c(I-);
(6)根据盖斯定律来计算反应的焓变,目标反应=①×2-②,即热化学方程式为:2Mg(s)+TiCl4(1)=2MgCl2(s)+Ti(s)△H=-512kJ?mol-1,
故答案为:2Mg(s)+TiCl4(1)=2MgCl2(s)+Ti(s)△H=-512kJ?mol-1.
点评:本题综合考查氯气和氯水的性质,为高频考点,侧重学生的分析、计算能力的考查,题目较为综合,难度较大,注意把握题给信息,根据反应的现象判断生成物进而书写相关反应的方程式.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列物质按照氧化物、单质、碱、混合物、纯净物的顺序排列正确的是( )
| A、氯酸钾、碳单质、液态氯化钠、液氨、王水 |
| B、双氧水、稀有气体、碱式碳酸镁、硫酸铜溶液、明矾 |
| C、烧碱、纯碱、火碱、天然气、乙酸 |
| D、二氧化锰、硫单质(S8)、NH3?H2O、纯净空气、H2O和D2O组成的混合物 |
 NO2
NO2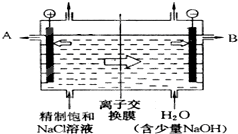 工业上电解制烧碱的技术是用离子交换膜法,主要原料是饱和食盐水.如图为离子交换膜法电解原理示意图:
工业上电解制烧碱的技术是用离子交换膜法,主要原料是饱和食盐水.如图为离子交换膜法电解原理示意图:
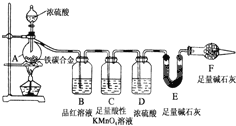 现有铁、碳两种元素组成的合金,某实验小组为了研究该合金的性质并测定该合金中碳的质量分数,设计了如下实验装置和实验方案.
现有铁、碳两种元素组成的合金,某实验小组为了研究该合金的性质并测定该合金中碳的质量分数,设计了如下实验装置和实验方案.