题目内容
| |||||||||||||||
答案:
解析:
解析:
(1) |
设起始时C(N2)=a C(H2)=b N2+3H2 起始浓度(mol/L) a b 0 转化浓度(mol/L) 2.5 7.5 5 平衡浓度(mol/L) 3.5 11 5…………………………(2分) |
(2) |
C(N2)=a=2.5 mol/L+3.5 mol/L=6 mol/L……………………(1分) C(H2)=b=11 mol/L+7.5 mol/L=18.5 mol/L………………………(1分) |
(3) |
N2的转化率= |

练习册系列答案
相关题目
 ………………(2分)
………………(2分) 2NH3,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示:
2NH3,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示: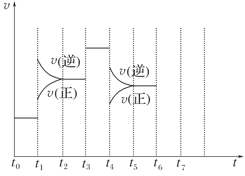
 2NH3已达到平衡状态的是
2NH3已达到平衡状态的是 2NH3,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示:
2NH3,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示: