题目内容
10.下列说法不正确的是( )| A. | 乙烯、乙炔、乙醛都能使溴水或酸性KMnO4溶液褪色 | |
| B. | 可用加入NaOH溶液并加热,通过观察油层是否消失或变薄来鉴别苯和乙酸乙酯 | |
| C. | 可用H2SO4溶液、银氨溶液和碘水来检验淀粉液是否部分水解 | |
| D. | 油脂在热NaOH溶液中完全水解后,加入饱和食盐水,可观察到液面上有固体析出 |
分析 A.均含不饱和键,与溴水发生加成,与高锰酸钾发生氧化反应;
B.苯与NaOH不反应,乙酸乙酯与NaOH反应后不分层;
C.检验淀粉液是否部分水解,需要在碱性条件下检验葡萄糖;
D.油脂在热NaOH溶液中完全水解后,生成高级脂肪酸钠,加饱和食盐水,发生盐析.
解答 解:A.乙烯、乙炔、乙醛都能与溴水或酸性KMnO4溶液发生加成或氧化反应,而使溴水或酸性KMnO4溶液褪色,故A正确;
B.NaOH溶液在加热条件下能使乙酸乙酯水解,油层会消失或变薄的是乙酸乙酯,故B正确;
C.淀粉溶液水解需要硫酸作催化剂,水解产物中需先加NaOH溶液中和至碱性,再滴加银氨溶液检验是否有葡萄糖,缺少试剂不能检验,故C错误;
D.油脂在热NaOH溶液中完全水解后,生成的高级脂肪酸钠密度小于食盐水,可观察到液面上有固体析出,故D正确;
故选C.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系、有机反应为解答的关键,侧重分析与应用能力的考查,注意有机物的性质及检验,题目难度不大.

练习册系列答案
相关题目
18.室温下,0.01mol/L二元酸H2A溶液的pH=3,下列说法正确的是( )
| A. | 该溶液中由水电离出的c(H+)为1.0×10-3mol/L | |
| B. | 在Na2A、NaHA两种溶液中,离子种类不同 | |
| C. | 在NaHA溶液中一定有c(OH-)+c(HA-)+2c(A2-)═c(Na+)+c(H+) | |
| D. | 在Na2A溶液中,c(Na+)>c(HA-)>c(A2-)>c(OH-)>c(H+) |
5.下列反应为氧化还原反应,且氧化剂和还原剂为同种物质的是( )
| A. | SO2+Cl2+2H2O=H2SO4+2HCl | B. | 3CO2+4NaOH=2NaHCO3+Na2CO3+H2O | ||
| C. | Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO | D. | 2NO2+2NaOH=NaNO2+NaNO3+H2O |
15.下列反应的离子方程式正确的是( )
| A. | 氢氧化钙溶液与少量碳酸氢镁溶液反应:Ca2++OH-+HCO3-═CaCO3↓+H2O | |
| B. | 向次氯酸钙溶液中通入少量SO2:Ca2++2ClO-+H2O+SO2═CaSO3↓+2HClO | |
| C. | Ca(HCO3)2溶液中加入过量NaOH溶液:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O | |
| D. | 硫酸亚铁的酸性溶液中加入H2O2溶液:Fe2++H2O2+2H+═Fe3++2H2O |
2.常温下,某溶液中由水电离出的c(H+)与c(OH-)的乘积为10-10,该溶液可能是( )
| A. | 一定浓度的CH3COONa溶液 | B. | 一定浓度的氨水溶液 | ||
| C. | 一定浓度的NaHSO4溶液 | D. | pH等于5的醋酸溶液 |
19.有NaCl、FeCl2、FeCl3、MgCl2、AlCl3五种溶液,用一种试剂就可把它们鉴别开来,这种试剂是( )
| A. | 盐酸 | B. | 烧碱溶液 | C. | 氨水 | D. | KSCN溶液 |
15.物质的量浓度相同的NaCl、MgCl 2、AlCl 3 三种溶液,当溶液的体积比为1:2:3时,用相同物质的量浓度的AgNO3 溶液将Cl-完全沉淀,则需AgNO3溶液的体积比为( )
| A. | 1:1:1 | B. | 3:4:3 | C. | 1:4:9 | D. | 1:2:3 |
 2,3-二甲基戊烷
2,3-二甲基戊烷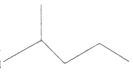 表示的分子式C6H14;
表示的分子式C6H14;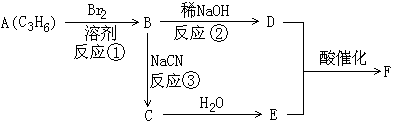
 .
.