题目内容
已知可逆反应:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ?mol-1,如图各图表示上述可逆反应建立平衡的过程及改变某一条件后建立起新的平衡过程的曲线:
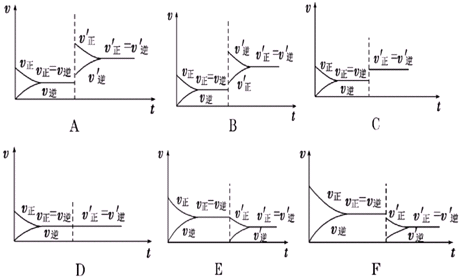
(1)固定容积加入稀有气体后的平衡图为
(2)降低温度后的平衡图为
(3)体系加压后的平衡图为
(4)升高温度后的平衡图为
(5)减小生成物浓度后的平衡图为
(6)加入催化剂后的平衡图为 .

(1)固定容积加入稀有气体后的平衡图为
(2)降低温度后的平衡图为
(3)体系加压后的平衡图为
(4)升高温度后的平衡图为
(5)减小生成物浓度后的平衡图为
(6)加入催化剂后的平衡图为
考点:化学反应速率变化曲线及其应用
专题:化学平衡专题
分析:升高温度,正逆反应速率都瞬时增大,平衡向着吸热的分析移动;增大压强,正逆反应速率都瞬时增大,平衡向着吸热的分析移动;增大反应物浓度,正反应速率瞬时增大,平衡正向移动;使用催化剂,正逆反应速率都瞬时增大,平衡不一定.
解答:
解:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ?mol-1,
(1)固定容积加入稀有气体后,正逆反应速率不变,平衡不移动,故对应图象为D;
故答案为:D;
(2)降低温度后,正逆反应速率都瞬时减小,平衡正向移动,故对应图象为F;
故答案为:F;
(3)体系加压后,正逆反应速率都瞬时增大,平衡正向移动,故对应图象为A;
故答案为:A;
(4)升高温度后,正逆反应速率都瞬时增大,平衡逆向移动,故对应图象为B;
故答案为:B;
(5)减小生成物浓度后,正反应速率瞬时不变,逆反应速率瞬时减小,平衡正向移动,故对应图象为E;
故答案为:D;
(6)加入催化剂后,正逆反应速率都瞬时增大,平衡不移动,故对应图象为C;
故答案为:C.
(1)固定容积加入稀有气体后,正逆反应速率不变,平衡不移动,故对应图象为D;
故答案为:D;
(2)降低温度后,正逆反应速率都瞬时减小,平衡正向移动,故对应图象为F;
故答案为:F;
(3)体系加压后,正逆反应速率都瞬时增大,平衡正向移动,故对应图象为A;
故答案为:A;
(4)升高温度后,正逆反应速率都瞬时增大,平衡逆向移动,故对应图象为B;
故答案为:B;
(5)减小生成物浓度后,正反应速率瞬时不变,逆反应速率瞬时减小,平衡正向移动,故对应图象为E;
故答案为:D;
(6)加入催化剂后,正逆反应速率都瞬时增大,平衡不移动,故对应图象为C;
故答案为:C.
点评:本题考查化学反应速率和化学平衡的影响因素,难度不大,要注意结合速率的变化和平衡移动的方向进行分析判断.

练习册系列答案
相关题目
常温时,下列关于电解质溶液的叙述正确的是( )
| A、稀释pH=10的氨水,溶液中所有离子的浓度均降低 |
| B、pH均为5的盐酸和硫酸氢钠溶液中,水的电离程度相同 |
| C、等物质的量浓度的①NH4HSO4②NH4Cl ③CH3COONH4④(NH4)2SO4c(NH4+)的大小顺序是 ①②③④ |
| D、分别中和pH与体积均相同的硫酸和醋酸,硫酸消耗氢氧化钠的物质的量多 |