��Ŀ����
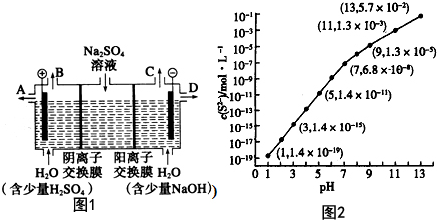
�¶�ΪTʱ���� 2.0 L�����ܱ������г���1.0 mol PCl5����ӦPCl5(g)  PCl3(g)+Cl2(g)����һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ�IJ������ݼ��±���
PCl3(g)+Cl2(g)����һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ�IJ������ݼ��±���
t / s | 0 | 50 | 150 | 250 | 350 |
n | 0 | 0��16 | 0��19 | 0��20 | 0��20 |
����˵����ȷ����
A����Ӧ��ǰ50s��ƽ������v(PCl3)=0��0032mol��L-1��s-1
B�����������������䣬�����¶ȣ�ƽ��ʱc(PCl3)=0��11mol��L-1����Ӧ�ġ�H<0
C����ͬ�¶��£���ʼʱ�������г���1��0molPCl5��0��20molPCl3��0��20molCl2����Ӧ�ﵽƽ��ǰv(��)��v(��)
D����ͬ�¶��£���ʼʱ�������г���2��0molPCl3��2��0molCl2���ﵽƽ��ʱ��PCl3��ת����С��80%
��ϰ��ϵ�д�
�����Ŀ
19������˵����ȷ���ǣ�������
| A�� | �������ܷ���ˮ�ⷴӦ�����Ҵ��Ͷ�����̼ | |
| B�� | �������ᡢ����ϩ���Ҷ������ɷ����ۺϷ�Ӧ | |
| C�� | ʵ��������������Ũ���ᡢ170���������Ʊ���ϩ | |
| D�� | �����ܸ�̼������Һ��Ӧ�����ӵ����Ա�̼��ǿ |
 (PCl3) / mol
(PCl3) / mol

 ֮��
֮��