题目内容
一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生NO2(g)+SO2(g)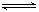 SO3(g)+NO(g)的可逆反应,下列能说明反应达到平衡状态的是( )
SO3(g)+NO(g)的可逆反应,下列能说明反应达到平衡状态的是( )
A.体系压强保持不变 B.混合气体颜色保持不变
C.SO3和NO的体积比保持不变 D.每消耗1 mol SO3的同时生成1 mol NO2
练习册系列答案
 春雨教育同步作文系列答案
春雨教育同步作文系列答案
相关题目
某同学用NaHCO3和KHCO3组成的混合物进行实验,测得如下数据(盐酸的物质的量浓度相等)。下列分析推理正确的是
盐酸 | 50 mL | 50 mL | 50 mL |
m(混合物) | 9.2 g | 14.2 g | 27.6 g |
V(CO2)(标准状况) | 2.24 L | 3.36 L | 3.36 L |
A.盐酸的物质的量浓度为3.0 mol/L
B.当混合物质量为9.2 g时,50 mL盐酸恰好完全反应
C.混合物中NaHCO3、KHCO3的物质的量之比为1∶2
D.混合物中NaHCO3的质量分数为45.7 %



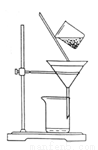
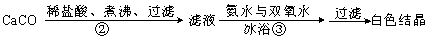
 Si + 2CO;②Si + 2Cl2
Si + 2CO;②Si + 2Cl2 SiCl4;③SiCl4 + 2H2
SiCl4;③SiCl4 + 2H2 Si + 4HCl,其中反应①和③属于( )
Si + 4HCl,其中反应①和③属于( ) 2 C6H5OH+CO32—;
2 C6H5OH+CO32—; Fe(OH) 2+2H+若在此溶液中加入盐酸后,用文字说明溶液颜色的变化及原因__________________.
Fe(OH) 2+2H+若在此溶液中加入盐酸后,用文字说明溶液颜色的变化及原因__________________.