题目内容
反应aA(g)+bB(g)?cC(g)+dD(g) 在容积不变的密闭容器中达到化学平衡,且起始时A与B的物质的量之比为a:b,则:
(1)达到平衡后,A、B的转化率之比是 .
(2)达到平衡后,若升高温度,C的质量分数降低,则该反应的正反应是 热反应.
(3)若同等倍数地增大A、B的物质的量浓度,并在原温度下达到平衡时,A与B的转化率也同时增大,则(a+b)与(c+d)的关系是(a+b) (c+d).(填“>”、“<”、或“=”)
(1)达到平衡后,A、B的转化率之比是
(2)达到平衡后,若升高温度,C的质量分数降低,则该反应的正反应是
(3)若同等倍数地增大A、B的物质的量浓度,并在原温度下达到平衡时,A与B的转化率也同时增大,则(a+b)与(c+d)的关系是(a+b)
考点:化学平衡的影响因素
专题:化学平衡专题
分析:(1)起始时A与B的物质的量之比为a:b,等于化学计量数之比,平衡时A与B的转化率相等;
(2)若升高温度,C的质量分数降低,平衡向逆反应方向移动,逆反应是吸热反应;
(3)同时同等倍数地增大A、B的浓度,等效为增大压强,A与B的转化率同时增大,平衡向正反应移动.
(2)若升高温度,C的质量分数降低,平衡向逆反应方向移动,逆反应是吸热反应;
(3)同时同等倍数地增大A、B的浓度,等效为增大压强,A与B的转化率同时增大,平衡向正反应移动.
解答:
解:(1)起始时A与B的物质的量之比为a:b,等于化学计量数之比,平衡时A与B的转化率相等,即平衡时A与B的转化率之比是1:1,故答案为:1:1;
(2)若升高温度,C的质量分数降低,平衡向逆反应方向移动,逆反应是吸热反应,正反应为放热反应,故答案为:放;
(3)同时同等倍数地增大A、B的浓度,等效为增大压强,A与B的转化率同时增大,平衡向正反应移动,增大压强平衡向气体体积减小的方向移动,故a+b>c+d,
故答案为:>.
(2)若升高温度,C的质量分数降低,平衡向逆反应方向移动,逆反应是吸热反应,正反应为放热反应,故答案为:放;
(3)同时同等倍数地增大A、B的浓度,等效为增大压强,A与B的转化率同时增大,平衡向正反应移动,增大压强平衡向气体体积减小的方向移动,故a+b>c+d,
故答案为:>.
点评:本题考查平衡移动、外界条件对平衡的影响、等效平衡等,难度不大,注意基础知识的理解掌握.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
某有机物的结构简式为CH2=C(CH3)-COOH,它不能发生的反应的是( )
| A、加成反应 | B、聚合反应 |
| C、酯化反应 | D、银镜反应 |
下表是元素周期表的一部分,有关说法正确的是( )
| 族 周期 |
IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 2 | c | d | |||||
| 3 | a | b | e | f |
| A、e的氢化物比d的氢化物稳定 |
| B、a、b、e三种元素的原子半径:e>b>a |
| C、六种元素中,c元素组成的单质和氧化物都是原子晶体 |
| D、c、e、f的最高价氧化物对应的水化物的酸性依次增强 |
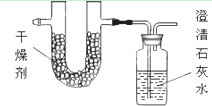 某烃CxHy同温同压条件下测得其蒸汽的密度是H2的43倍;将a g该烃完全燃烧,并使产生的产物全部依次通过下图装置,得到下表所列的实验结果(假设产生的气体产物完全被吸收).
某烃CxHy同温同压条件下测得其蒸汽的密度是H2的43倍;将a g该烃完全燃烧,并使产生的产物全部依次通过下图装置,得到下表所列的实验结果(假设产生的气体产物完全被吸收).