题目内容
15.当0.2mol烃A在足量氧气中完全燃烧时生成CO2和H2O各1.2mol,催化加氢后生成2,2-二甲基丁烷,则A的结构简式为(CH3)3C-CH=CH2.分析 根据C元素、H元素守恒确定该烃的分子式为C6H12,在催化剂作用下与H2发生加成反应,生成2,2-二甲基丁烷,则该烃的结构简式为(CH3)3C-CH=CH2.
解答 解:当0.2mol烃A在足量氧气中完全燃烧时生成CO2和H2O各1.2mol,n(烃):n(C):n(H)=n(烃):n(CO2):2n(H2O)=0.2mol:1.2mol:1.2mol×2=1:6:12,即1个分子中含有6个C原子、12个H原子,故该烃的分子式为C6H12,在催化剂作用下与H2发生加成反应,生成2.2-二甲基丁烷,则该烃的结构简式为:(CH3)3C-CH=CH2,(或表示为 ),为3,3-二甲基-1-丁烯,
),为3,3-二甲基-1-丁烯,
故答案为:(CH3)3C-CH=CH2.
点评 本题考查了有机物分子式、结构简式的确定,题目难度不大,注意能够根据质量守恒定律以及烯烃的性质确定有机物分子式、结构简式.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
13.下列关于有机物的叙述正确的是( )
| A. | 治疗疟疾的青蒿素(如图),分子式为C15H20O5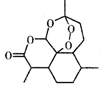 | |
| B. | 甲苯苯环上的一个氢原子被-C3H6Cl取代,形成的同分异构体有9种 | |
| C. | 对三联苯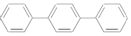 分子中至少有16个原子共平面 分子中至少有16个原子共平面 | |
| D. | 油脂和乙烯在一定条件下都能与水反应,且反应类型相同 |
14.下列各组物质不能用NaOH鉴别的是( )
| A. | Fe2+和Fe3+ | B. | 酚酞试液和水 | C. | 盐酸和硝酸 | D. | NH4Cl和KCl |
10.某实验小组配制0.10mol/LNaOH溶液并进行有关性质实验,回答下列问题.
(1)若实验中大约要使用475mLNaOH溶液,至少需要称量NaOH固体2.0g.
(2)从如图中选择称量NaOH固体所需要的仪器是(填字母)abe.
(3)下列情况会使所配溶液浓度偏低的是(填序号)①③⑤⑦
①称量读数时,左盘高,右盘低
②所用的砝码生锈
③溶液转移到容量瓶后,未进行洗涤操作
④转移溶液前容量瓶内有少量蒸馏水
⑤定容时,仰视容量瓶的刻度线
⑥在烧杯中溶解NaOH后,立即将所得溶液注入容量瓶中
⑦定容后摇匀,发现液面降低,又补加少量水,重新达到刻度实验室欲配制
⑧用量筒量取一定量浓硫酸配制稀硫酸,转移到烧杯后,用少量水洗涤量筒.
(1)若实验中大约要使用475mLNaOH溶液,至少需要称量NaOH固体2.0g.
(2)从如图中选择称量NaOH固体所需要的仪器是(填字母)abe.
| 名称 | 托盘天平 (带砝码) | 小烧杯 | 坩埚钳 | 玻璃棒 | 药匙 | 量筒 |
| 仪器 | 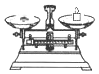 |  |  |  |  |  |
| 序号 | a | b | c | d | e | f |
①称量读数时,左盘高,右盘低
②所用的砝码生锈
③溶液转移到容量瓶后,未进行洗涤操作
④转移溶液前容量瓶内有少量蒸馏水
⑤定容时,仰视容量瓶的刻度线
⑥在烧杯中溶解NaOH后,立即将所得溶液注入容量瓶中
⑦定容后摇匀,发现液面降低,又补加少量水,重新达到刻度实验室欲配制
⑧用量筒量取一定量浓硫酸配制稀硫酸,转移到烧杯后,用少量水洗涤量筒.
20.茶叶中含有多种有益于人体健康的有机成分及钙、铁等微量金属元素,某化学研究性学习小组设计方案用以检验某品牌茶叶中铁元素的存在并测定钙元素的质量分数 (已知CaC2O4为白色沉淀物质).首先取200g茶叶样品进行如图1操作:请回答下列有关问题: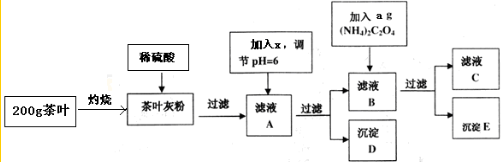
(1)①文献资料显示,某些金属离子的氢氧化物完全沉淀的pH为:
②(NH4)3C2O4溶液显酸性
实验前要先将茶叶样品高温灼烧程灰粉,这部操作需要用到的实验仪器有:酒精灯、三脚架、玻璃棒、BC、其主要目的是使样品中的有机物完全分解.
A.蒸发皿 B.坩埚 C.泥三角 D.石棉网
(2)从滤液A→沉淀D的过程中需要加入的物质X可以选择C
A.CaO B.Ca(OH)2 C.NH3•H2O
(3)用KMnO4标准溶液滴定C溶液时所发生的反应为:5C2O42-+2MnO4-+16H+=10CO2↑+2Mn2++8H2O
现将滤液C稀释至250mL,再取其中的25.00mL溶液,用硫酸酸化后,用0.10mol•L-1的KMnO4标准溶液滴定,终点时消耗KMnO4溶液体积如下表所示:
①此步操作过程中需要用到下列哪些仪器(如图)CDE(填写序号);
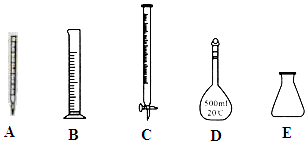
②滴定达到终点时的现象是滴入最后一滴KMnO4,溶液由无色变为紫色,且半分钟不恢复原色.
③为保证实验精确度,沉淀D及E需要分别洗涤,并将洗涤液转移回母液中,若不洗涤沉淀洗涤沉淀D,会使测定钙元素的含量偏低.(填“偏低”“偏高”、“无影响”,下同)若不洗涤沉淀E,会使测定钙元素的含量偏高.
④原茶叶中钙元素的质量分数为$\frac{\frac{a}{124}-0.05}{5}$.(用含a的代数式表示)
(4)设计最简单的实验检验茶叶中含有铁元素的操作和现象是:取少量的滤液A,滴入硫氰化钾溶液,溶液变成红色,证明溶液中存在铁离子,也证明离子茶叶中含有铁元素.

(1)①文献资料显示,某些金属离子的氢氧化物完全沉淀的pH为:
| 离子 | Ca2+ | Fe3+ |
| 完全沉淀时的pH | 13 | 4.1 |
实验前要先将茶叶样品高温灼烧程灰粉,这部操作需要用到的实验仪器有:酒精灯、三脚架、玻璃棒、BC、其主要目的是使样品中的有机物完全分解.
A.蒸发皿 B.坩埚 C.泥三角 D.石棉网
(2)从滤液A→沉淀D的过程中需要加入的物质X可以选择C
A.CaO B.Ca(OH)2 C.NH3•H2O
(3)用KMnO4标准溶液滴定C溶液时所发生的反应为:5C2O42-+2MnO4-+16H+=10CO2↑+2Mn2++8H2O
现将滤液C稀释至250mL,再取其中的25.00mL溶液,用硫酸酸化后,用0.10mol•L-1的KMnO4标准溶液滴定,终点时消耗KMnO4溶液体积如下表所示:
| 编号 | 终点时消耗KMnO4溶液体积(mL) |
| 1 | 19.98 |
| 2 | 22.00 |
| 3 | 20.02 |

②滴定达到终点时的现象是滴入最后一滴KMnO4,溶液由无色变为紫色,且半分钟不恢复原色.
③为保证实验精确度,沉淀D及E需要分别洗涤,并将洗涤液转移回母液中,若不洗涤沉淀洗涤沉淀D,会使测定钙元素的含量偏低.(填“偏低”“偏高”、“无影响”,下同)若不洗涤沉淀E,会使测定钙元素的含量偏高.
④原茶叶中钙元素的质量分数为$\frac{\frac{a}{124}-0.05}{5}$.(用含a的代数式表示)
(4)设计最简单的实验检验茶叶中含有铁元素的操作和现象是:取少量的滤液A,滴入硫氰化钾溶液,溶液变成红色,证明溶液中存在铁离子,也证明离子茶叶中含有铁元素.
4.电化学在日常生活中用途广泛,图甲是镁--次氯酸钠燃料电池,电池总反应为:Mg+ClO-+H2O=Cl-+Mg(OH)2↓,图乙是含Cr2O72-的工业废水的处理.下列说法正确的是( )
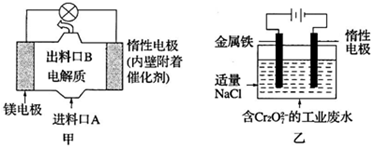

| A. | 图乙中Cr2O72-向惰性电极移动,与该极附近的OH-结合转化成Cr(OH)3除去 | |
| B. | 图甲中发生的还原反应是Mg2++ClO-+H2O+2e-=Cl-+Mg(OH)2↓ | |
| C. | 图乙电解池中,若有0.84g阳极材料参与反应,则阴极会有3.36L的气体产生 | |
| D. | 若图甲燃料电池消耗0.36g镁产生的电量用以图乙废水处理,理论上可产生1.07g氢氧化铁沉淀 |
 按要求回答问题:
按要求回答问题: ;
;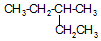 的系统命名为3-甲基戊烷.
的系统命名为3-甲基戊烷. .
. ,如果要合成
,如果要合成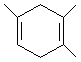 ,所用的原料可以是
,所用的原料可以是