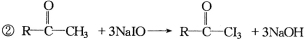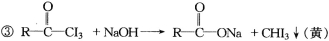题目内容
电解熔融氯化钙可以得到金属钙和氯气,钙在氯气中燃烧又能生成氯化钙.请你根据已学知识,按如图箭头所表示的物质间可能发生的转化,分析下列说法中正确的是
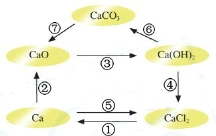
A.CaO、Ca(OH)2、CaCO3都含有氧元素,所以CaO、Ca(OH)2、CaCO3都属于氧化物
B.电解熔融氯化钙得到金属钙和氯气的反应既是氧化还原反应又是化合反应
C.虽然碳酸钙的水溶液不导电,但碳酸钙是电解质
D.工业上以氯气和石灰水为原料通过反应④生产漂白粉
C
【解析】
试题分析:氧化物只能含两种元素,Ca(OH)2、CaCO3含有3种元素,故A项错误;电解熔融氯化钙得到金属钙和氯气,是一种物质生成两种物质,属于是分解反应,故B错误;碳酸钙属于盐,酸碱盐都是电解质,故C正确;工业上以氯气和石灰乳为原料生产漂白粉,故D错误。
考点:本题考查化学基本概念。

练习册系列答案
相关题目
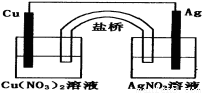
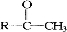 与NaOH溶液、碘水三者混和后可发生如下反应:
与NaOH溶液、碘水三者混和后可发生如下反应: NaI + NaIO + H2O
NaI + NaIO + H2O