题目内容
能正确表示下列反应的离子方程式是
A.Cl2通入NaOH溶液:Cl2 + OH- =Cl- + ClO- + H2O
B.NaHCO3溶液中加入稀盐酸:CO32- + 2H+ =CO2↑ + H2O
C.AlCl3溶液中加入过量稀氨水:Al3+ + 4NH3·H2O =AlO2- + 4NH4+ + 2H2O
D.Cu溶于稀硝酸:3Cu + 8H+ + 2NO3- =3Cu2+ + 2NO↑ + 4H2O
选修3——物质结构与性质]
X、Y、Z、W、Q、R均为前四周期元素,且原子序数依次增大。其相关信息如下表所示:
X元素的基态原子中电子分布在三个不同的能级中,且每个能级中的电子总数相同 |
Y元素的气态氢化物与其最高价氧化物对应的水化物能发生化合反应 |
Z元素的族序数是其周期数的三倍 |
W原子的第一至第六电离能分别为: I1=578KJ·mol-1 I2=1817KJ·mol-1 I3=2745KJ·mol-1 I4=11575KJ·mol-1 I5=14830KJ·mol-1 I6=18376KJ·mol-1 |
Q为前四周期中电负性最小的元素 |
元素R位于周期表的第10列 |
回答下列问题:
(1)Y元素的基态原子的电子排布式为_____________,其第一电离能比Z元素原子的第一电离能________(填“高”或“低”)
(2)X的氯化物的熔点比Q的氯化物的熔点_______________(填“高”或“低”),理由是___________________
(3)光谱证实元素W的单质与强碱性溶液反应有W(OH)4]-生成,则W(OH)4]-中存在_______(填字母)
a.极性共价键 b.非极性共价键 c.配位键 d.氢键
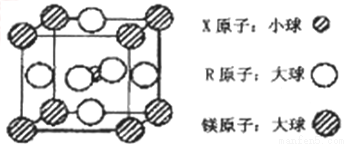
(4)含有X、R和镁三种元素的某种晶体具有超导性,其结构如下图所示。则该晶体的化学式为_________;晶体中每个镁原子周围距离最近的R原子有___________个。



 CH3COOH)+c(CH3COO-):① = ②
CH3COOH)+c(CH3COO-):① = ② C.置换反应 D.复分解反应
C.置换反应 D.复分解反应 CH3OCH3(g)+ 3H2O(g) △H<0
CH3OCH3(g)+ 3H2O(g) △H<0 状态的是 (选填编号,注意大小写)
状态的是 (选填编号,注意大小写)