题目内容
下列盐溶液能发生水解的用离子方程式表示,不能发生水解的写“不发生水解”字样,并说明溶液的酸碱性
K2CO3 ,溶液呈 性;
Na2SO4 ,溶液呈 性;
CuCl2 ,溶液呈 性.
K2CO3
Na2SO4
CuCl2
考点:离子方程式的书写,盐类水解的应用
专题:盐类的水解专题
分析:先判断是否有弱离子再确定是否水解,结合水解方程式判断溶液的酸碱性.
解答:
解:K2CO3是强碱弱酸盐,水解后水溶液呈碱性,水解离子方程式为:CO32-+H2O?HCO3-+OH-;
Na2SO4是强酸强碱盐,不水解,溶液呈中性;
CuCl2是强酸弱碱盐,水解后溶液呈酸性,水解离子方程式为:Cu2++2H2O?Cu(OH)2+2H+,
故答案为:CO32-+H2O?HCO3-+OH-;碱;不发生水解;中;Cu2++2H2O?Cu(OH)2+2H+;酸.
Na2SO4是强酸强碱盐,不水解,溶液呈中性;
CuCl2是强酸弱碱盐,水解后溶液呈酸性,水解离子方程式为:Cu2++2H2O?Cu(OH)2+2H+,
故答案为:CO32-+H2O?HCO3-+OH-;碱;不发生水解;中;Cu2++2H2O?Cu(OH)2+2H+;酸.
点评:本题考查盐类水解,题目难度不大,注意把握盐类水解规律:有弱(弱离子)才水解,无弱(弱离子)不水解,谁弱(弱离子)谁水解,谁强显谁性(酸碱性).

练习册系列答案
相关题目
在铜锌电池中,下列叙述正确的是( )
| A、正极附近硫酸根离子浓度增大 |
| B、负极附近硫酸根离子浓度减小 |
| C、正极附近硫酸根离子浓度减小 |
| D、若锌片、铜片同时有气泡冒出,说明锌不纯 |
对下列有机反应类型的认识中,不正确的是( )
A、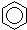 +HNO3 +HNO3
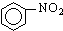 +H2O;取代反应 +H2O;取代反应 | |||
| B、CH4+Cl2→CH3Cl+HCl;置换反应 | |||
C、CH2═CH2+H2O
| |||
D、2CH3CH2OH+O2
|
有甲酸、乙酸、乙醛、乙酸乙酯、乙醇、溴乙烷6种无色溶液,只用一种试剂就可以将它们一一鉴别出来.这种试剂是( )
| A、蒸馏水 |
| B、FeCl3溶液 |
| C、新制Cu(OH)2悬浊液 |
| D、NaOH溶液 |
 A、T、X、Y、Z是中学化学常见的四种元素,原子序数依次增大,其结构或性质信息如下表:
A、T、X、Y、Z是中学化学常见的四种元素,原子序数依次增大,其结构或性质信息如下表: :
:
 纳米技术制成的金属燃料、非金属固体燃料、氢气等已应用到社会生活和高科技领域.
纳米技术制成的金属燃料、非金属固体燃料、氢气等已应用到社会生活和高科技领域.