题目内容
3.下列物质中主要成分为纤维素的是( )| A. | 尼龙 | B. | 黏胶纤维 | C. | 硝化纤维 | D. | 醋酸纤维 |
分析 根据黏胶纤维的主要成分为纤维素;尼龙的主要成分为有机高分子材料;硝化纤维是纤维素与硝酸酯化反应的产物;醋酸纤维是纤维素与醋酸酯化反应的产物来解答.
解答 解:A.尼龙是人工合成的有机高分子材料,故A错误;
B.黏胶纤维中主要成分为纤维素,故B正确;
C.硝化纤维是纤维素与硝酸酯化反应的产物,主要成分为硝化纤维,故C错误;
D.醋酸纤维是纤维素与醋酸酯化反应的产物,主要成分为醋酸纤维,故D错误;
故选B.
点评 本题考查纤维素的用途,明确物质的制备与组成是解题的关键,难度不大.

练习册系列答案
相关题目
13.在一定温度下,下列叙述中属于可逆反应A(g)+B(g)?2C(g)达到平衡标志的是( )
| A. | 单位时间内生成a mol A的同时消耗2a mol C | |
| B. | 混合气体的压强不再变化 | |
| C. | 单位时间内消耗a mol A的同时消耗a mol B | |
| D. | B气体的浓度不再发生变化 |
11.下列各组离子中,在给定条件下能够大量共存的是( )
| A. | 通入足量CO2后的溶液中:Na+、SiO32-、CH3COO-、CO32- | |
| B. | 中性溶液中:Fe3+、MnO4-、SO42-、K+ | |
| C. | 酸性溶液中:Na+、ClO-、SO42-、I- | |
| D. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=1012的溶液中:NH4+、Al3+、NO3-、Cl- |
8.现有几组物质的熔点(℃)数据:
(1)A组属于原子晶体,其熔化时克服的微粒间的作用力是共价键.
(2)B组晶体共同的物理性质是①②③④(填序号).
①有金属光泽 ②导电性 ③导热性 ④延展性
(3)C组中HF熔点反常是由于HF分子间能形成氢键,其熔化时需要消耗的能量更多.
(4)D组晶体可能具有的性质是②④(填序号).
①硬度小 ②水溶液能导电 ③固体能导电 ④熔融状态能导电
(5)D组晶体的熔点NaCl>KCl,其原因解释为:NaCl>KCl都为离子晶体,r(Na+)<r(K+),在离子所带电荷相同的情况下,半径越小,晶格能越大,熔点就越高.
| A组 | B组 | C组 | D组 |
| 金刚石:3550 | Li:181 | HF:-83 | NaCl:801 |
| 硅晶体:1410 | Na:98 | HCl:-115 | KCl:776 |
| 硼晶体:2300 | K:64 | HBr:-89 | RbCl:718 |
| 二氧化硅:1723 | Rb:39 | HI:-51 | CaCl:645 |
(2)B组晶体共同的物理性质是①②③④(填序号).
①有金属光泽 ②导电性 ③导热性 ④延展性
(3)C组中HF熔点反常是由于HF分子间能形成氢键,其熔化时需要消耗的能量更多.
(4)D组晶体可能具有的性质是②④(填序号).
①硬度小 ②水溶液能导电 ③固体能导电 ④熔融状态能导电
(5)D组晶体的熔点NaCl>KCl,其原因解释为:NaCl>KCl都为离子晶体,r(Na+)<r(K+),在离子所带电荷相同的情况下,半径越小,晶格能越大,熔点就越高.
2.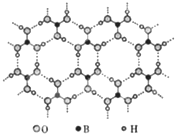 正硼酸(H3BO3)是一种层状结构白色晶体,层内的H3BO3分子通过氢键相连(如图).下列有关说法错误的是( )
正硼酸(H3BO3)是一种层状结构白色晶体,层内的H3BO3分子通过氢键相连(如图).下列有关说法错误的是( )
 正硼酸(H3BO3)是一种层状结构白色晶体,层内的H3BO3分子通过氢键相连(如图).下列有关说法错误的是( )
正硼酸(H3BO3)是一种层状结构白色晶体,层内的H3BO3分子通过氢键相连(如图).下列有关说法错误的是( )| A. | 正硼酸晶体属于分子晶体 | B. | H3BO3分子的稳定性与氢键有关 | ||
| C. | 分子中硼原子最外层不是8e-结构 | D. | 含1mol H3BO3的晶体中有3mol氢键 |
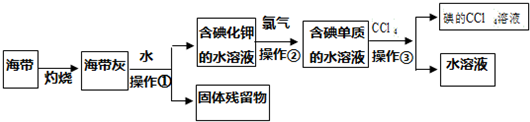

 双氧水最主要的用途是漂白和杀菌消毒,在环境保护、化学合成和工业生产中有着广泛的应用.查阅资料得知:工业上用电解KHSO4饱和溶液制取H2O2,如图所示.
双氧水最主要的用途是漂白和杀菌消毒,在环境保护、化学合成和工业生产中有着广泛的应用.查阅资料得知:工业上用电解KHSO4饱和溶液制取H2O2,如图所示.