题目内容
7.氧化还原反应在生产、生活中具有广泛用途,贯穿古今.(1)水是人体的重要组成部分,是人体中含量最多的一种物质.
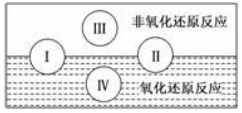
试写出有水参加的符合反应类型Ⅳ的一个化学方程式:2Na+2H2O=2NaOH+H2↑,其中水为氧化剂.
(2)氯化铵常用于焊接. 如:在焊接铜器时用氯化铵除去铜器表面的氧化铜以便焊接,其反应为:
4CuO+2NH4Cl═3Cu+1CuCl2+1N2+4+H2O
①配平此氧化还原反应方程式.
②该反应中,被氧化的元素是氮(填元素名称),氧化剂是CuO(填化学式).
③反应中若产生0.2mol的气体,则有1.2NA个电子转移.
分析 (1)由图可知,Ⅳ为有水参加的氧化还原反应;
(2)反应中Cu由+2价降低为0,N元素的化合价由-3价升高为0,转移6mol电子,由电子守恒、原子守恒分析.
解答 解:(1)由图可知,Ⅳ为有水参加的氧化还原反应,如2Na+2H2O=2NaOH+H2↑,水中H元素的化合价降低,则水为氧化剂,
故答案为:2Na+2H2O=2NaOH+H2↑;氧化;
(2)①Cu由+2价降低为0,N元素的化合价由-3价升高为0,由电子守恒、原子守恒可知,NH4Cl失去3个电子,而铜得到2个电子,得失电子守恒,NH4Cl前面系数为2,铜前面的系数为3,再结合原子守恒可知,反应为4CuO+2NH4Cl=3Cu+CuCl2+N2+4H2O,故答案为:4;2;3;1;1;4;
②N元素失去电子被氧化,Cu元素得到电子,则CuO为氧化剂,故答案为:氮;CuO;
③由反应可知,生成1mol气体转移6mol电子,则产生0.2mol的气体转移的电子为0.2mol×6×NA=1.2NA,故答案为:1.2NA.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念及转移电子的考查,题目难度不大.

练习册系列答案
相关题目
17.镧镍合金在一定条件下可吸收氢气形成氢化物:LaNi5(s)+3H2(g)?LaNi5H6(s)△H<0,欲使LaNi5H6(s)释放出气态氢,根据平衡移动原理,可改变的条件是( )
| A. | 增加LaNi5H6(s)的量 | B. | 降低温度 | ||
| C. | 减小压强 | D. | 使用催化剂 |
18.下列物质既能跟盐酸反应,又能跟NaOH溶液反应的是( )
①Al
②Al2O3
③Al(OH)3
④Na2CO3溶液
⑤Ca(HCO3)2溶液
⑥KHSO4溶液.
①Al
②Al2O3
③Al(OH)3
④Na2CO3溶液
⑤Ca(HCO3)2溶液
⑥KHSO4溶液.
| A. | ①②③⑥ | B. | ①②③④ | C. | ①②③⑤ | D. | ①②③④⑤ |
15.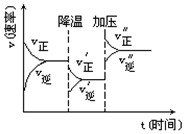 如图是可逆反应A+2B?2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断( )
如图是可逆反应A+2B?2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断( )
 如图是可逆反应A+2B?2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断( )
如图是可逆反应A+2B?2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断( )| A. | 降温后逆反应速率增大 | B. | 逆反应是放热反应 | ||
| C. | A、B、C、D均为气体 | D. | 若A、B是气体,则D是液体或固体 |
2.下列各组物质,按化合物、单质、混合物的顺序排列的是( )
| A. | 烧碱、液态氧、碘酒 | B. | 干冰、铁、冰水混合物 | ||
| C. | 生石灰、白磷、熟石灰 | D. | 碱石灰、氮气、胆矾 |
12.下列关于金属的腐蚀及防腐说法错误的是( )
| A. | 马口铁(镀锡铁)镀层破损铁的腐蚀速率加快 | |
| B. | 为了防止钢铁设备腐蚀,利用外加电流的阴极保护法,应另附加一惰性电极,惰性电极作阴极 | |
| C. | 可以采用改变金属组成或结构的方法防止金属腐蚀 | |
| D. | 为保护海轮的船壳,利用牺牲阳极的阴极保护法,常在船壳上镶入锌块 |
19.绿色能源是指使用时不会对环境造成污染的能源.下列属于绿色能源的是( )
①太阳能②风能③石油④煤⑤木材⑥潮汐能.
①太阳能②风能③石油④煤⑤木材⑥潮汐能.
| A. | ①②③ | B. | ③④ | C. | ④ | D. | ①②⑥ |
9.25℃时,5种银盐的溶度积常数(Ksp)分别是:
下列说法正确的是( )
| AgCl | Ag2SO4 | Ag2S | AgBr | AgI |
| 1.8×10-10 | 1.4×10-5 | 6.3×10-50 | 7.7×10-13 | 8.51×10-16 |
| A. | 氯化银、溴化银和碘化银的溶解度依次增大 | |
| B. | 将硫酸银溶解于水后,向其中加入少量硫化钠固体,不能得到黑色沉淀 | |
| C. | 在5mL1.5×10-5 mol•L-1的NaCl溶液中,加入1滴(1mL约20滴)1.0×10-3mol•L-1的AgNO3溶液,不能观察到白色沉淀 | |
| D. | 在烧杯中放入6.24 g 硫酸银固体,加200 g 水,经充分溶解后,所得饱和溶液的体积为200 mL,溶液中Ag+ 的物质的量浓度为0.2 mol•L-1 |
10. 合成气(C0+H2)在煤化工和天然气化工中有着十分重要的地位,由合成气可合成多种有机基础原料和产品.
合成气(C0+H2)在煤化工和天然气化工中有着十分重要的地位,由合成气可合成多种有机基础原料和产品.
(一)煤化工生产中生产合成气的反应为:C(s)+H20(g)?C0(g)+H2(g)△H1
已知:C(s)+$\frac{1}{2}$O2(g)=C0(g)△H2=-110.5kJ•mol-1
H2(g)+$\frac{1}{2}$02(g)=H20(g)△H3=-242kJ•mol-1
(1 )反应C(s)+H20(g)?C0(g)+H2(g)在高温(填高温或低温)下自发进行,理由是△H1=△H2-△H3=131.5kJ>0,△S>0.
(2)在恒温恒容下,同时放入C(s)、H20(g)、CO(g)、H2(g)四种物质,下列事实能够说明反应C(s)+H20(g)?C0(g)+H2(g))已达到平衡的是ACD.
A.反应体系中,混合气体的密度不再改变
B.反应体系中,各组分的物质的量相等
C.反应体系中,当有2molH-0键断裂的同时有1molH-H键断裂
D.混合气体的平均相对分子质量为18且保持不变
(二)天然气化工中生产合成气的主要反应为:
2CH4(g)+02(g)?2C0(g)+4H2(g)△H=-23kJ•mol-1
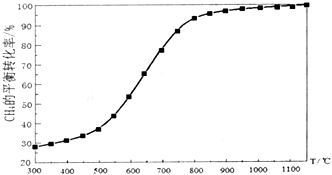
在恒容容器中按物质的量之比1:2加入一定量的CH4和O2,在压强为1.01×105Pa、不同温度下测得CH4的平衡转化率如图所示:
(3)图中所表示的CH4的平衡转化率随温度变化的曲线,实质上是多个反应共同作用的结果.与之相关的反应还有以下三个反应:
I.CH4(g)+2O2(g)?C02(g)+2H20(g)△H5=-802kJ•mol-1
Ⅱ.CH4(g)+H2O(g)?C0(g)+3H2(g)△H6=+201kJ•mol-1
Ⅲ.CO(g)+H2O(g)?CO2(g)+H2(g)△H7=-35kJ•mol-1
你认为上述反应中,在高温下占主导地位的是Ⅱ(填反应序号).
(4)根据平衡移动原理,请在图中画出压强为5.05×105Pa时CH4的平衡转化率随温度的变化曲线.
(5)工业上常用选择性来判断不同反应条件下目标产物的产率,即:选择性=$\frac{目标产物的产率}{反应原料的转化率}$,现有实验测得反应2CH4(g)+02(g)?2CO(g)+4H2(g)在750℃下,以不同碳氧比[$\frac{n(C{H}_{4})}{n({O}_{2})}$]投料时反应达平衡后CH4的转化率及H2、CO的选择性,所测数据如表所示:
最佳碳氧比[$\frac{n(C{H}_{4})}{n({O}_{2})}$]为1:0.5.假设按碳氧比[$\frac{n(C{H}_{4})}{n({O}_{2})}$]=l:1投料,反应容器的体积为VL,通入CH4和02各amol,请列式表示平衡时容器内C0的浓度(用a、V的代数式表示)$\frac{a×0.98×0.65}{V}$mol/L.
 合成气(C0+H2)在煤化工和天然气化工中有着十分重要的地位,由合成气可合成多种有机基础原料和产品.
合成气(C0+H2)在煤化工和天然气化工中有着十分重要的地位,由合成气可合成多种有机基础原料和产品.(一)煤化工生产中生产合成气的反应为:C(s)+H20(g)?C0(g)+H2(g)△H1
已知:C(s)+$\frac{1}{2}$O2(g)=C0(g)△H2=-110.5kJ•mol-1
H2(g)+$\frac{1}{2}$02(g)=H20(g)△H3=-242kJ•mol-1
(1 )反应C(s)+H20(g)?C0(g)+H2(g)在高温(填高温或低温)下自发进行,理由是△H1=△H2-△H3=131.5kJ>0,△S>0.
(2)在恒温恒容下,同时放入C(s)、H20(g)、CO(g)、H2(g)四种物质,下列事实能够说明反应C(s)+H20(g)?C0(g)+H2(g))已达到平衡的是ACD.
A.反应体系中,混合气体的密度不再改变
B.反应体系中,各组分的物质的量相等
C.反应体系中,当有2molH-0键断裂的同时有1molH-H键断裂
D.混合气体的平均相对分子质量为18且保持不变
(二)天然气化工中生产合成气的主要反应为:
2CH4(g)+02(g)?2C0(g)+4H2(g)△H=-23kJ•mol-1
在恒容容器中按物质的量之比1:2加入一定量的CH4和O2,在压强为1.01×105Pa、不同温度下测得CH4的平衡转化率如图所示:
(3)图中所表示的CH4的平衡转化率随温度变化的曲线,实质上是多个反应共同作用的结果.与之相关的反应还有以下三个反应:
I.CH4(g)+2O2(g)?C02(g)+2H20(g)△H5=-802kJ•mol-1
Ⅱ.CH4(g)+H2O(g)?C0(g)+3H2(g)△H6=+201kJ•mol-1
Ⅲ.CO(g)+H2O(g)?CO2(g)+H2(g)△H7=-35kJ•mol-1
你认为上述反应中,在高温下占主导地位的是Ⅱ(填反应序号).
(4)根据平衡移动原理,请在图中画出压强为5.05×105Pa时CH4的平衡转化率随温度的变化曲线.
(5)工业上常用选择性来判断不同反应条件下目标产物的产率,即:选择性=$\frac{目标产物的产率}{反应原料的转化率}$,现有实验测得反应2CH4(g)+02(g)?2CO(g)+4H2(g)在750℃下,以不同碳氧比[$\frac{n(C{H}_{4})}{n({O}_{2})}$]投料时反应达平衡后CH4的转化率及H2、CO的选择性,所测数据如表所示:
| 碳氧比[$\frac{n(C{H}_{4})}{n({O}_{2})}$] | 1:0.25 | 1:0.5 | 1:1 | 1:1.25 |
| CH4转化率 | 0.40 | 0.88 | 0.98 | 0.99 |
| H2选择性 | 0.98 | 0.93 | 0.67 | 0.40 |
| CO选择性 | 0.99 | 0.94 | 0.65 | 0.32 |