题目内容
通常情况,下列气体能大量共存的是( )
| A、NO、O2 |
| B、SO2、H2S |
| C、NH3、HCl |
| D、H2、O2 |
考点:氮的氧化物的性质及其对环境的影响,氨的化学性质,二氧化硫的化学性质,硫化氢
专题:元素及其化合物
分析:常温下,能相互反应的气体不能共存;反之,气体之间不反应,能共存,以此来解答.
解答:
解:A.常温下NO、O2反应生成二氧化氮,不能共存,故A不选;
B.常温下SO2、H2S反应生成硫单质和水,不可以共存,故B不选;
C.NH3、HCl常温下反应生成氯化铵,则不可以共存,故C不选;
D.反应需要在点燃或加热下进行,常温下不反应,则可以共存,故D选;
故选D.
B.常温下SO2、H2S反应生成硫单质和水,不可以共存,故B不选;
C.NH3、HCl常温下反应生成氯化铵,则不可以共存,故C不选;
D.反应需要在点燃或加热下进行,常温下不反应,则可以共存,故D选;
故选D.
点评:本题考查物质的共存,把握物质的性质及反应的条件为解答的关键,注意常温下反应不能共存,题目难度不大.

练习册系列答案
相关题目
下列电离方程式书写正确的是( )
| A、H2S?2H++S2- | ||
| B、H2S+H2O?H3O++HS- | ||
C、NH3+H2O═NH
| ||
| D、HClO═H++ClO |
下列反应属于取代反应的是( )
| A、C2H4通入溴水中,溴水褪色 |
| B、C2H4通入KMnO4酸性溶液中,溶液褪色 |
| C、苯与溴水混合后振荡,水层褪色 |
| D、CH4与Cl2的混合气体光照后颜色变浅 |
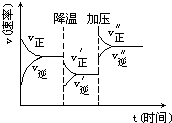 图是可逆反应A+2B?2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断( )
图是可逆反应A+2B?2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断( )| A、正反应是吸热反应 |
| B、若A、B是气体,则D是液体或固体 |
| C、加压反应向逆方向进行 |
| D、A、B、C、D均为气体 |
下列数量的物质中含原子个数最多的是( )
| A、0.4mol 氧气 |
| B、4℃时,5.4mLH2O |
| C、标况下5.6L 二氧化碳 |
| D、10 g 氖 |
有机物A的结构简式为 ,A的同分异构体中带苯环的化合物(烯醇结构除外)共有( )
,A的同分异构体中带苯环的化合物(烯醇结构除外)共有( )
 ,A的同分异构体中带苯环的化合物(烯醇结构除外)共有( )
,A的同分异构体中带苯环的化合物(烯醇结构除外)共有( )| A、3种 | B、4种 | C、5种 | D、6种 |
下列说法正确的是( )
A、c(H+)=
| ||
| B、将水加热,KW增大,pH不变,仍呈中性 | ||
| C、向水中加入少量硫酸氢钠固体,溶液的c(H+) 增大,平衡逆向移动,KW减小 | ||
| D、向0.1 mol?L-1醋酸溶液中加水,溶液中水电离产生的c(H+) 将减小 |
常温条件下,一密闭容器中以1:2:3的比例充入NO、N2、NO2,在条件不变的情况下,向容器中充入与NO2等体积的O2,充分反应后,有关容器中的气体的下列叙述中正确的是(不考虑NO2转化为N2O4)( )
| A、NO、N2、NO2、O2的体积比为1:2:3:3 |
| B、N2、NO2、O2的体积比为2:3:2 |
| C、NO、NO2、O2的体积比为4:3:1 |
| D、N2、NO2、O2的体积比为4:8:5 |
标准状况下,将4.48L的NO2和NO组成的混合气体通入100mL的水中,气体体积缩小为2.24L,假设溶液的体积不变,则下列说法中错误的是( )
| A、所得溶液中溶质的物质的量浓度为1.0mol?L-1 |
| B、剩余气体中氮元素与氧元素的质量为8:7 |
| C、原混合气体中NO2和NO的体积比为1:1 |
| D、反应过程中转移的电子总数为0.1mol |