题目内容
智利硝石矿层中含有碘酸钠,可用亚硫酸氢钠与其反应来制备单质,其化学反应式为:2NaIO3+5NaHSO3====3NaHSO4+2Na2SO4+I2+H2O(1)反应中_________元素被氧化,_________是氧化剂。
(2)标出电子转移方向和数目_________。
(3)从反应产物中,所得氧化产物与还原产物质量之比为_________。
解析:解答氧化还原反应的有关问题,应先从化合价的变化入手,找出电子转移的方向,![]() ;再根据化合价的改变与有关概念的联系即可作答。在任何一个氧化还原反应中,得失电子总数(电子转移总数)等于化合价升降总数,本题第(2)问即是根据此规律来确定电子转移总数的。
;再根据化合价的改变与有关概念的联系即可作答。在任何一个氧化还原反应中,得失电子总数(电子转移总数)等于化合价升降总数,本题第(2)问即是根据此规律来确定电子转移总数的。
(3)氧化产物为3NaHSO4+2Na2SO4,还原产物为I2,故氧化产物与还原产物质量之比为(3×120+2×142)∶(2×127)=322∶127。
答案:(1)硫 碘酸钠
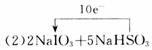
(3)322∶127

练习册系列答案
相关题目