题目内容
9.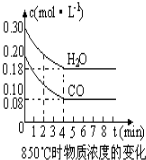 在一体积为10L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:CO(g)+H2O(g)?CO2(g)+H2 (g)△H<0,CO和H2O浓度变化如图.
在一体积为10L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:CO(g)+H2O(g)?CO2(g)+H2 (g)△H<0,CO和H2O浓度变化如图.t℃时物质浓度(mol•L-1)的变化:
| 时间(min) | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
(2)850℃时,此反应的平衡常数K=1,若保持温度、体积不变,起始时CO和H2O的浓度均为0.2mol•L-1,则达平衡时CO的转化率为50%.在850℃时,若上述反应体系中各物质浓度为C(CO)=0.07mol•L-1C(H2O)=0.17mol•L-1C( CO2)=0.13mol•L-1C(H2)=0.13mol•L-1,则此时该反应向逆方向移动.
(3)t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如上表.
①表中3min~4min之间反应处于平衡状态; c 1数值大于0.08mol•L-1 (填大于、小于或等于)
②反应在4min~5min间,平衡向逆方向移动,可能的原因是d (单选),表中5min~6min之间数值发生变化,可能的原因是a (单选)
a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度.
分析 (1)根据v=$\frac{△c}{△t}$计算;
(2)分别计算各物质的平衡浓度,根据平衡常数表达式计算K;温度不变,不变,设转化COx,列三段式用x表示k,得x再计算转化率;计算加入量的Qc,与k比较得反应方向;
(3)根据浓度、压强、温度对平衡移动的影响分析.
解答 解:(1)由图象可知,v(CO)=$\frac{0.2mol/L-0.08mol/L}{4min}$=0.03mol/(L•min);
故答案为:0.03;
(2)根据三段式:
CO(g)十H2O(g)?CO2(g)十H2 (g)
起始:0.20mol/L 0.30mol/L 0 0
转化:0.12mol/L 0.12mol/L 0.12mol/L 0.12mol/L
平衡:0.08mol/L 0.18mol/L 0.12mol/L 0.12mol/L
则K=$\frac{c(C{O}_{2})•c({H}_{2})}{c(CO)•c({H}_{2}O)}$=$\frac{0.12×0.12}{0.08×0.18}$=1;起始时CO和H2O的浓度均为0.2mol•L-1,设反应CO浓度x,根据三段式:
CO(g)十H2O(g)?CO2(g)十H2 (g)
起始:0.20mol/L 0.2mol/L 0 0
转化:x mol/L x mol/L x mol/L x mol/L
平衡:(0.2-x)mol/L (0.2-x)mol/L x mol/L x mol/L
温度不变,k不变,则有$\frac{{x}^{2}}{(0.2-x)^{2}}$=1,解得x=0.1,故CO的转化率为$\frac{0.1}{0.2}$×100%=50%;若上述反应体系中各物质浓度为C(CO)=0.07mol•L-1C(H2O)=0.17mol•L-1C( CO2)=0.13mol•L-1C(H2)=0.13mol•L-1,则Qc=$\frac{0.13×0.13}{0.07×0.17}$=1.4>1,反应向着逆反应方向进行;
故答案为:1,50%,逆;
(3)①在高于850℃时发生反应,化学反应速率加快,一定在4min前达到化学平衡.另外从表中可看出反应在3min和4min时的各物质浓度相同,故3min-4min之间反应应处于平衡状态.由于是放热反应,温度升高,化学平衡向逆反应方向移动,C1数值应大于0.08 mol/L.
故答案为:平衡;大于;
②反应在4min-5min间,平衡向逆方向移动可能是升高温度、增大生成物浓度、减少反应物浓度等因素引起,故选d.表中5min-6min之间CO浓度减少,H2O浓度增大,CO2浓度增大,只有增加水蒸气,使化学平衡向正反应方向移动.故选a,
故答案为:d;a.
点评 本题综合考查化学平衡常数、平衡的有关计算和判断等问题,题目难度较大,将图表信息和图象信息相结合来分析是解答的关键,较好的考查学生的能力.

 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案| A. | Na2CO3→NaHCO3 | B. | MnO4-→Mn2+ | C. | Cu→CuO | D. | H2O2→H2O |
(1)在密闭器中,该反应达到平衡后,测得如表数据.
| 实验序号 | 温度(℃) | 初始CCl4浓度(mol•L-1) | 初始H2浓度(mol•L-1) | CCl4的平衡转化率 |
| 1 | 110 | 1 | 1 | 50% |
| 2 | 100 | 1 | 1 | X |
| 3 | 110 | 0.8 | Y | 60% |
②实验2中,X的值B(填序号).
A.等于50% B.大于50% C.小于50% D.无法确定
③实验3中的Y值为1.2.
(2)为从平衡体系CCl4+H2?CHCl3+HCl中分离得到CHCl3,请你结合题给信息设计合理的方案,用简要的文字表示:先把平衡体系中的混合物降温到61.2℃以下得到CCl4和CHCl3液态混合物,再分馏得到CHCl3.
(1)洗涤滴定管前必须首先检漏.
(2)选用盐酸作为标准溶液进行测定实验.将盐酸装入滴定管,NaOH溶液装入锥形瓶,滴加甲基橙/酚酞作指示剂.滴定时,眼睛注视锥形瓶中溶液颜色的变化,当锥形瓶内溶液由黄色变橙色/红色变无色、且在半分钟内不褪去即达滴定终点.记录此时滴定管内液面读数V(末).
(3)实验数据记录及处理:
标准盐酸浓度:0.1054mol/L
| 实验次数 | 待测氢氧化钠溶液体积(mL) | 标准盐酸体积(mL) | NaOH溶液浓度(mol/L) | ||
| 初读数 | 末读数 | 体积 | |||
| 1 | 20.00 | 0.50 | 20.70 | 20.20 | 0.1059 |
| 2 | 20.00 | 6.00 | 26.00 | 20.00 | |
(4)若测定结果偏低,原因可能是ACD.
A、见到指示剂的颜色有变化就停止滴定
B、锥形瓶用蒸馏水清洗后,未用待装液润洗
C、读数时,若滴定前视线偏低,滴定后视线偏高
D、滴定前滴定管的尖嘴部分充满液体,滴定终点时尖嘴部分有气泡.
| A. | 乙烯分子中C═C双键中有一个键容易断裂 | |
| B. | 乙烯分子中6个原子共平面 | |
| C. | 不能用酸性高锰酸钾溶液除去乙烷中混有的乙烯 | |
| D. | 乙烷和乙烯都能使溴水褪色 |
| A. | 升高温度 | B. | 加入催化剂 | C. | .增大H2(g)的浓度 | D. | 增大NH3(g)的浓度 |