题目内容
16.下列离子在溶液中能大量共存的是( )| A. | Al3+、Ba2+、OH-、SO42- | B. | Ca2+、H+、Cl-、CO32- | ||
| C. | H+、Ba2+、Ag+、Cl- | D. | K+、OH-、Na+、NO3- |
分析 A.铝离子与氢氧根离子、钡离子与硫酸根离子反应;
B.钙离子、氢离子都与碳酸根离子反应;
C.银离子与氯离子反应生成难溶物氯化银;
D.四种离子之间不反应,能够共存.
解答 解:A.Al3+与OH-、Ba2+与SO42-之间发生反应,在溶液中不能大量共存,故A错误;
B.Ca2+、H+都与CO32-反应,在溶液中不能大量共存,故B错误;
C.Ag+、Cl-之间反应生成氯化银沉淀,在溶液中不能大量共存,故C错误;
D.K+、OH-、Na+、NO3-之间不发生反应,在溶液中不能大量共存,故D正确;
故选D.
点评 本题考查离子共存的正误判断,为高考的高频题,题目难度中等,注意掌握离子反应发生条件,明确离子不能大量共存的一般情况,如:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;试题侧重对学生基础知识的训练和检验,有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
相关题目
6.常温下,向10mL 0.1mol/L的HR溶液中逐滴滴人0.1mol/L的NH3•H2O溶液,所得溶液pH及导电性变化如图.下列分析不正确的是( )
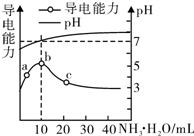

| A. | a~b点导电能力增强说明HR为弱酸 | |
| B. | b点溶液pH=7说明NH4R没有水解 | |
| C. | c点溶液存在c( NH4+)>c( R-)、c(OH-)>c(H+) | |
| D. | b~e任意点溶液均有c(H+)×c(OH-)=Kw=l.0×l0-14 |
4.下列用来表示物质变化的反应式中,正确的是( )
| A. | 钢铁腐蚀时可能发生的正极反应:2H2O+O2+4e-═4OH- | |
| B. | 常温下,NaHCO3溶液显碱性:HCO3-+H2O?CO32-+H3O+ | |
| C. | 氢氧化镁与稀硫酸反应:H++OH-═H2O | |
| D. | 硫酸亚铁酸性溶液中加入过氧化氢:Fe2++H2O2+2H+═Fe3++2H2O |
8.常温下,在20mL0.1mol/L Na2CO3溶液中逐滴加入0.1mol/L 盐酸40mL,溶液的pH逐渐降低,此时溶液中含碳元素的微粒物质的量浓度的百分含量(纵轴)也发生变化(CO2因逸出未画出),如图所示.下列说法不正确的是( )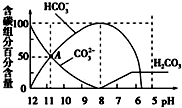

| A. | 0.1 mol/L Na2CO3溶液中c(Na+)+c(H+)═2c(CO32-)+c(HCO3-)+c(OH-) | |
| B. | 当加入20 mL盐酸时,混合溶液的pH约为8 | |
| C. | 常温下CO2饱和溶液的pH约为5.6 | |
| D. | 在A点:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |
14.下列化学用语表示正确的是( )
| A. | 硫原子的结构示意图: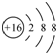 | |
| B. | 乙烯的结构简式:CH2CH2 | |
| C. | 二氧化碳分子的电子式: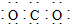 | |
| D. | 硫酸钠的电离方程式:Na2SO4═2Na++SO42- |
15.某同学用滤纸折成一个纸蝴蝶并喷洒一种溶液(保持湿润),挂在铁架台上.另取一只盛某种溶液的烧杯,放在纸蝴蝶的下方.过一会,发现纸蝴蝶变为红色.下表的组合中,能够实现上述变化的是( )
| A | B | C | D | |
| 纸蝴蝶上的喷洒液 | 石蕊 | 石蕊 | 酚酞 | 石蕊 |
| 小烧杯中的溶液 | 浓盐酸 | 浓氨水 | NaOH溶液 | 浓硫酸 |
| A. | A | B. | B | C. | C | D. | D |