题目内容
18.NA为阿伏加德罗常数的值.下列说法正确的是( )| A. | 1molCu与足量的S反应转移电子数为2NA | |
| B. | 46g有机物C2H6O中含有共价键的数目为7NA | |
| C. | 在0.5L2mol•L-1的Na2CO3溶液中含CO32-的数目为NA | |
| D. | 10gD2O和H218O的混合物中含有的中子数为5NA |
分析 A.铜与硫反应生成硫化亚铜;
B.依据n=$\frac{m}{M}$计算物质的量,结合有机物C2H6O存在同分异构体分析;
C.碳酸根离子为弱酸根离子,部分发生水解;
D.质量转化为物质的量,结合1个D2O和H218O中都含有10个中子解答.
解答 解:A.1molCu与足量的S反应生成0.5mol硫化亚铜,转移电子数为NA,故A错误;
B.依据n=$\frac{m}{M}$计算物质的量=$\frac{46g}{46g/mol}$=1mol,有机物C2H6O存在同分异构体,若为乙醇含有极性键的数目一定为7NA,若为甲醚含有极性键的数目一定为8NA,故B错误;
C.碳酸根离子为弱酸根离子,部分发生水解,在0.5L2mol•L-1的Na2CO3溶液中含CO32-的数目小于NA,故C错误;
D.10gD2O和H218O的混合物物质的量为$\frac{10g}{10g/mol}$=0.5mol,含有的中子物质的量为0.5mol×10=5mol,个数为5NA,故D正确;
故选:D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,注意碳酸根离子的水解,注意铜与弱氧化剂反应生成亚铜离子.

练习册系列答案
 小学课时特训系列答案
小学课时特训系列答案
相关题目
8.用NA为阿伏加罗常数的值,下列说法正确的是( )
| A. | 标准状况下,2.24LCHCl3中含有碳氯键数目为0.3NA | |
| B. | 25℃时,0.1mol/L的Na2CO3溶液中含有Na+的数目为0.02NA | |
| C. | 28gN2和CO的混合气体中含有的分子数为NA | |
| D. | 1molNa2O和1molNa2O2的混合物中,含有的离子总数为7NA |
9.煤、石油、天然气是人类使用的主要能源,同时也是重要的化工原料,下列不属于以煤、石油和天然气为主要原料生产的合成材料是( )
| A. | 塑料 | B. | 玻璃 | C. | 淀粉 | D. | 合成纤维 |
6.通常情况下,氯化钠、氯化艳、二氧化碳和二氧化硅的晶体结构分别如图所示:
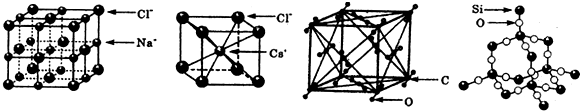
下列关于这些晶体结构和性质的叙述不正确的是( )

下列关于这些晶体结构和性质的叙述不正确的是( )
| A. | 干冰的晶胞中含有6个CO2分子 | |
| B. | 干冰是分子晶体,其中不仅存在分子间作用力,而且也存在共价键 | |
| C. | 在二氧化硅晶体中,平均每个Si原子形成4个Si-O共价单键 | |
| D. | 同一主族的元素与另一相同元素所形成的化学式相似的物质不一定具有相同的晶体结构 |
13.下列各溶液中,微粒的物质的量浓度关系正确的是( )
| A. | 0.lmol/LCH3COONa溶液:c(Na+)═c(CH3COO-) | |
| B. | 0.1mol/LNa2CO3溶液:c(Na+)═c(HCO3-)+2c(CO32-)+2c(H2CO3) | |
| C. | 向醋酸钠溶液加适量醋酸所得溶液:c(Na+)+c(H+)═c(CH3COO-)+c(OH-) | |
| D. | 常温下,将pH=2的盐酸和pH=12的氨水等体积混合:c(Cl-)>c(NH4+) |
3. 氨是一种重要的化工产品.
氨是一种重要的化工产品.
(1)热化学循环制氢可以采用如下的反应:
①Br2(g)+CaO(s)=CaBr2(s)+$\frac{1}{2}$O2(g)△H=-73kJ•mol-1
②CaBr2(s)+H2O(g)=CaO(s)+2HBr(g)△H=+212kJ•mol-1
③Fe3O4(s)+8HBr(g)=Br2(g)+3FeBr2(s)+4H2O(g)△H=-274kJ•mol-1
④3FeBr2(s)+4H2O(g)=Fe3O4(s)+6HBr(g)+H2(g)△H=+354kJ•mol-1
则H2O(g)??H2(g)+$\frac{1}{2}$O2(g)△H=+249kJ•mol-1.
(2)在一定温度下,在固定体积的密闭容器中进行可逆反应:N2(g)+3H2(g)??2NH3(g)△H=-92.4kJ•mol-1.可判定该可逆反应达到平衡状态标志的选项是BDE.
A.v(N2)正=2v(NH3)逆
B.单位时间生成amolN2的同时消耗3amolH2
C.混合气体的密度不再随时间变化
D.容器内的总压强不再随时间而变化
E.amolN≡N键断裂的同时,有6amolN-H键断裂
F.N2、H2、NH3的分子数之比为1:3:2
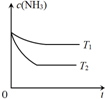
(3)反应2NH3(g)??N2(g)+3H2(g)在容积为1.0L的密闭容器中进行,NH3的初始浓度为0.05mol/L.温度T1和T2下NH3的浓度与时间关系如图所示.回答下列问题:
①上述反应的温度T1小于T2,平衡常数K(T1)小于K(T2).(填“大于”、“小于”或“等于”)
②若温度T2时,5min后反应达到平衡,NH3的转化率为80%,则:平衡时混合气体总的物质的量为0.09mol.反应在0~5min区间的平均反应速率v(N2)=0.004mol/(L•min).
(4)某化学小组模拟工业合成氨的反应.在容积固定为2L的密闭容器内充入1molN2和3molH2,加入合适催化剂(体积可以忽略不计)后在一定温度压强下开始反应,并用压力计监测容器内压强的变化如下:
则反应在该温度下平衡常数K=2.37(保留三三位有效数字);保持温度不变,30min时再向该密闭容器中投入0.5molN2、0.5molH2和1molNH3,此时反应将正向进行(填“正向进行”、“逆向进行”或“处于平衡状态”).
(5)以氨为燃料可以设计制造氨燃料电池,产物无污染.若电极材料均为惰性电极,KOH溶液作电解质溶液,则该电池负极电极反应式为2NH3-6e-+6OH-=N2+6H2O.
 氨是一种重要的化工产品.
氨是一种重要的化工产品.(1)热化学循环制氢可以采用如下的反应:
①Br2(g)+CaO(s)=CaBr2(s)+$\frac{1}{2}$O2(g)△H=-73kJ•mol-1
②CaBr2(s)+H2O(g)=CaO(s)+2HBr(g)△H=+212kJ•mol-1
③Fe3O4(s)+8HBr(g)=Br2(g)+3FeBr2(s)+4H2O(g)△H=-274kJ•mol-1
④3FeBr2(s)+4H2O(g)=Fe3O4(s)+6HBr(g)+H2(g)△H=+354kJ•mol-1
则H2O(g)??H2(g)+$\frac{1}{2}$O2(g)△H=+249kJ•mol-1.
(2)在一定温度下,在固定体积的密闭容器中进行可逆反应:N2(g)+3H2(g)??2NH3(g)△H=-92.4kJ•mol-1.可判定该可逆反应达到平衡状态标志的选项是BDE.
A.v(N2)正=2v(NH3)逆
B.单位时间生成amolN2的同时消耗3amolH2
C.混合气体的密度不再随时间变化
D.容器内的总压强不再随时间而变化
E.amolN≡N键断裂的同时,有6amolN-H键断裂
F.N2、H2、NH3的分子数之比为1:3:2
(3)反应2NH3(g)??N2(g)+3H2(g)在容积为1.0L的密闭容器中进行,NH3的初始浓度为0.05mol/L.温度T1和T2下NH3的浓度与时间关系如图所示.回答下列问题:
①上述反应的温度T1小于T2,平衡常数K(T1)小于K(T2).(填“大于”、“小于”或“等于”)
②若温度T2时,5min后反应达到平衡,NH3的转化率为80%,则:平衡时混合气体总的物质的量为0.09mol.反应在0~5min区间的平均反应速率v(N2)=0.004mol/(L•min).
(4)某化学小组模拟工业合成氨的反应.在容积固定为2L的密闭容器内充入1molN2和3molH2,加入合适催化剂(体积可以忽略不计)后在一定温度压强下开始反应,并用压力计监测容器内压强的变化如下:
| 反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| 压强/MPa | 16.80 | 14.78 | 13.86 | 13.27 | 12.85 | 12.60 | 12.60 |
(5)以氨为燃料可以设计制造氨燃料电池,产物无污染.若电极材料均为惰性电极,KOH溶液作电解质溶液,则该电池负极电极反应式为2NH3-6e-+6OH-=N2+6H2O.
10.废铅蓄电池的一种回收利用工艺流程如图所示:
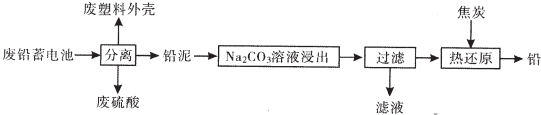
部分难溶电解质的性质如表:
回答下列问题:
(1)在生产、生活中使用广泛,铅蓄电池的缺点有比能量低(写一条).
(2)燃烧废塑料外壳可以发电,其一系列能量转换过程:化学能→热能→机械能→电能.
(3)将流程图中的废硫酸和滤液按一定比例混合,再将所得的混台液经蒸发浓缩、冷却结晶等操作,可以析出十水硫酸钠晶体.
(4)利用铅泥中的PbS04溶于CH3COONa溶液生成弱电解质(CH3COO)2Pb,(CH3COO)2Pb溶液与KC10在强碱性条件下反应制取Pb02,写出后一步生成PbO2的离子方程式(CH3COO)2Pb+ClO-+2OH-=Pb02↓+Cl-+2CH3COO-+H2O.
(5)25aC时,Na2CO3溶液浸出时发生的反应为:CO32-(aq)+PbSO4(s)?PbCO3(s)+SO42-(aq),计算该反应的平衡常数K=1.2×10-5.以滤渣PbCO3和焦炭为原料可制备金属铅,用化学方程式表示制备过程PbCO3$\frac{\underline{\;\;△\;\;}}{\;}$PbO+CO2↑、2PbO$\frac{\underline{\;\;△\;\;}}{\;}$2Pb+CO2↑
(6)已知Pb(OH)2是既能溶于稀硝酸,又能溶于KOH溶液的两性氢氧化物.设计实验区别PbCr04和BaCr04取少量待测物于两支试管中,分别与过量KOH溶液反应,能溶解的是PbCr04,不溶解的是BaCr04.

部分难溶电解质的性质如表:
| 物质 | Kap(25℃) | 颜色 |
| PbSO4 | 1.8×10-8 | 白色 |
| PbCO3 | 1.5×10-13 | 白色 |
| PbCrO4 | 1.8×10-14 | 黄色 |
| BaCrO4 | 1.2×10-10 | 黄色 |
| Pb(OH)2 | 1.8×10-20 | 白色 |
(1)在生产、生活中使用广泛,铅蓄电池的缺点有比能量低(写一条).
(2)燃烧废塑料外壳可以发电,其一系列能量转换过程:化学能→热能→机械能→电能.
(3)将流程图中的废硫酸和滤液按一定比例混合,再将所得的混台液经蒸发浓缩、冷却结晶等操作,可以析出十水硫酸钠晶体.
(4)利用铅泥中的PbS04溶于CH3COONa溶液生成弱电解质(CH3COO)2Pb,(CH3COO)2Pb溶液与KC10在强碱性条件下反应制取Pb02,写出后一步生成PbO2的离子方程式(CH3COO)2Pb+ClO-+2OH-=Pb02↓+Cl-+2CH3COO-+H2O.
(5)25aC时,Na2CO3溶液浸出时发生的反应为:CO32-(aq)+PbSO4(s)?PbCO3(s)+SO42-(aq),计算该反应的平衡常数K=1.2×10-5.以滤渣PbCO3和焦炭为原料可制备金属铅,用化学方程式表示制备过程PbCO3$\frac{\underline{\;\;△\;\;}}{\;}$PbO+CO2↑、2PbO$\frac{\underline{\;\;△\;\;}}{\;}$2Pb+CO2↑
(6)已知Pb(OH)2是既能溶于稀硝酸,又能溶于KOH溶液的两性氢氧化物.设计实验区别PbCr04和BaCr04取少量待测物于两支试管中,分别与过量KOH溶液反应,能溶解的是PbCr04,不溶解的是BaCr04.
8.下列化学用语表述一定正确的是( )
| A. | 甲醛的电子式: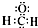 | |
| B. | 苯酚钠溶液中中通入少量二氧化碳气体: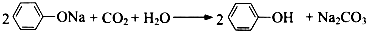 | |
| C. | 溴乙烷与氢氧化钠水溶液共热:C2H5Br+OH-$→_{△}^{H_{2}O}$CH2=CH2↑+Br-+H2O | |
| D. | 乙醇与灼热的氧化铜反应:CH3CH2OH+CuO$\stackrel{△}{→}$CH3CHO+Cu+H2O |
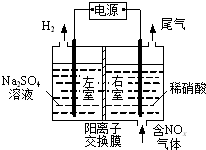 电解法处理含氮氧化物废气,可回收硝酸,具有较高的环境效益和经济效益.实验室模拟电解法吸收NOx的装置如图所示(图中电极均为石墨电极).
电解法处理含氮氧化物废气,可回收硝酸,具有较高的环境效益和经济效益.实验室模拟电解法吸收NOx的装置如图所示(图中电极均为石墨电极).