��Ŀ����
��8�֣�����������CO2���ڻ��ۣ���в����̬����������������ܵ�ȫ�����ע��
��1����ҵ�ϳ��ø�Ũ�ȵ�K2CO3 ��Һ����CO2������ҺX�������õ�ⷨʹK2CO3��Һ��������װ��ʾ��ͼ���£�
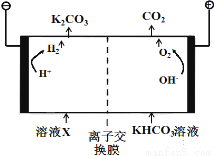
�������������ķ�Ӧ���� ��H ++ HCO3- == H2O + CO2����
��2������װ���в�����CO2��H2��һ�������·�Ӧ���ɼ״��Ȳ����ҵ�����ø÷�Ӧ�ϳɼ״���
��֪��25 �棬101 KPa�£�
H2(g) + 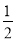 O2(g) === H2O(g) �� H1= ��242 kJ��mol��1
O2(g) === H2O(g) �� H1= ��242 kJ��mol��1
CH3OH(g) + O2(g) === CO2 (g) + 2 H2O(g) �� H2= ��676 kJ��mol��1
O2(g) === CO2 (g) + 2 H2O(g) �� H2= ��676 kJ��mol��1
�� д��CO2��H2������̬�״��Ȳ�����Ȼ�ѧ����ʽ ��
�� �����ʾ�ϳɼ״��ķ�Ӧ�������仯ʾ��ͼ��������ȷ���� ������ĸ��ţ���
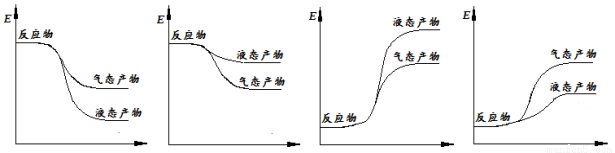
a b c d
��3������ȼ�ϵ����һ���������ォ��ѧ��ֱ��ת���ɵ��ܵ�װ�á���֪ij�ּ״�����ȼ�ϵ���У��������ҺΪ���ԣ�ʾ��ͼ���£�

�ٸõ�����·���ӵ���������Ϊ ����д����A��B����B��A������
��A�缫�����״������ĵ缫��ӦʽΪ ��
��1��4OH - - 4e- == 2H2O + O2����2�֣�
��2����CO2(g) + 3H2(g) == CH3OH(g) + H2O(g) ��H = ��50 kJ��mol��1��2�֣� �� a��1�֣�
��3�� �ٴ�A��B��1�֣� ��CH3OH + H2O - 6e- == 6H++ CO2����2�֣�
��������
�����������1�����������������ӷŵ�����������ˮ���缫��ӦʽΪ4OH--4e-�T2H2O+O2����
��2����H2��g��+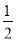 O2��g���TH2O��g����H1=-242kJ/mol�٣�CH3OH��g��+
O2��g���TH2O��g����H1=-242kJ/mol�٣�CH3OH��g��+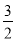 O2��g���TCO2��g��+2H2O��g����H2=-676kJ/mol�ڣ�������ʽ3��-�ڵ�CO2��g��+3H2��g���TCH3OH��g��+H2O��g����H=3����-242kJ/mol��-��-676kJ/mol��=-50 kJ/mol��
O2��g���TCO2��g��+2H2O��g����H2=-676kJ/mol�ڣ�������ʽ3��-�ڵ�CO2��g��+3H2��g���TCH3OH��g��+H2O��g����H=3����-242kJ/mol��-��-676kJ/mol��=-50 kJ/mol��
�ڸ÷�Ӧ�Ƿ��ȷ�Ӧ����Ӧ������������������������������Խ�ȶ���������ԽС������Һ̬���ʵ�����С����̬���ʣ������������ͼ����a����ѡa��
��3���ٸ�ȼ�ϵ���У��״�ʧ���ӷ���������Ӧ������A�Ǹ�����B�����������ӴӸ���A��������B���ʴ�Ϊ����A��B��
��A�缫�ϼ״�ʧ���Ӻ�ˮ��Ӧ���������ӺͶ�����̼���缫��ӦʽΪ��CH3OH+H2O-6e-�T6H++CO2����
���㣺����ԭ���ԭ������˹���ɡ����ԭ����

 ��˵����ȷ����
��˵����ȷ����