题目内容
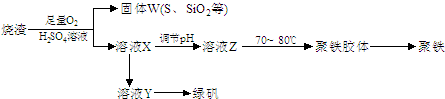
实验室欲测定绿矾中FeSO4·7H2O的质量分数。称1 g绿矾溶解在300 mL水中,再加入硫酸和磷酸。用0.02 mol·L-1 KMnO4溶液滴定到溶液变粉红色,消耗V mL。已知:(1)FeSO4·7H2O的质量分数____________________。
(2)简述磷酸的作用__________________________________________________。
解析:(1)设1 g绿矾中含FeSO4·7H2O的物质的量为x,由![]() +5Fe2++8H+====Mn2++5Fe3+
+5Fe2++8H+====Mn2++5Fe3+
+4H2O,可知x=5×V mL×10-3 L·mL-1×0.02 mol·L-1=V×10-4mol;m(FeSO4·7H2O)=V×10-4 mol×278 g·mol-1=2.78×10-2V g;绿矾中FeSO4·7H2O的质量分数为![]() ×100%=2.78V%。
×100%=2.78V%。
(2)氧化产物Fe3+使溶液呈棕黄色,干扰达到滴定终点粉红色的观察。由题目所给信息可知,加入H3PO4能与Fe3+结合生成无色物质,消除了Fe3+的干扰。
答案:(1)2.78V%
(2)磷酸和铁离子生成无色物质,可消除棕黄色的铁离子的干扰

练习册系列答案
相关题目