题目内容
黄铁矿(主要成分为FeS2)是我国大多数硫酸厂制取硫酸的主要原料.某化学学习小组对某黄铁矿石进行如下实验探究.[实验一]测定硫元素的含量.
Ⅰ、将m1g该黄铁矿样品放入如图1所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铁矿样品至反应完全.石英管中发生反应的化学方程式为:4FeS2+11O2 2Fe2O3+8SO2.
2Fe2O3+8SO2.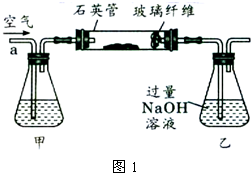
Ⅱ、反应结束后,将乙瓶中的溶液进行如图2所示处理.
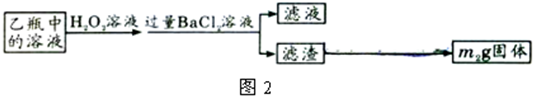
[实验二]测定铁元素的含量.
Ⅲ、测定铁元素含量的实验步骤如图3所示.
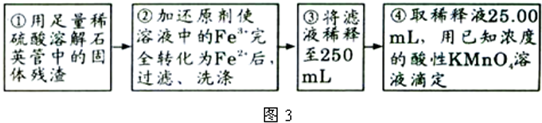
问题讨论:
(1)Ⅰ中,甲瓶内所盛试剂是______溶液.乙瓶内发生反应的离子方程式有:______、______.
(2)Ⅱ中的滤渣在称量前还应进行的操作是______.
(3)Ⅱ中,所加H2O2溶液(氧化剂)需足量的理由是______.
(4)④中取稀释液25.00ml需用的仪器是______.Ⅲ的步骤③中,需要用到的仪器除烧杯、玻璃棒、胶头滴管外,还有______(画出其简易装置图).
(5)该黄铁矿中硫元素的质量分数为______.
乙中二氧化硫和氢氧化钠反应生成亚硫酸钠,离子方程式为 SO2+2OH-=SO32-+H2O,亚硫酸钠和氧气反应生成硫酸钠,离子方程式为2SO32-+O2=2SO42-,
故答案为:NaOH;SO2+2OH-=SO32-+H2O;2SO32-+O2=2SO42-;
(2)为准确称量固体的质量,在称量之前需洗涤和干燥;故答案为:洗涤、干燥;
(3)为使亚硫酸根离子完全转化为硫酸根离子,加入的双氧水要足量,故答案为:使SO32-完全氧化为SO42-;
(4)④中取稀释液25.00ml,溶液是酸性溶液,体积数据要求到小数点后两位,需用的仪器是酸式滴定管,Ⅲ的步骤③中,一定物质的量浓度溶液的配制中,除了烧杯、玻璃棒、胶头滴管外,还需要250mL容量瓶,容量瓶装置图为:
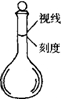 ,故答案为:酸式滴定管;250mL容量瓶;
,故答案为:酸式滴定管;250mL容量瓶;(5)最终所得沉淀是硫酸钡,根据硫原子守恒得硫的质量,设硫的质量为x,
S-----BaSO4
32g 233g
x m2g
x=
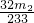 g
g质量分数=
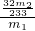 ×100%=
×100%=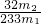 ×100%;
×100%;故答案为:
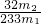 ×100%.
×100%.分析:(1)为防止二氧化碳的干扰,应将空气中的二氧化碳用碱液除掉;二氧化硫能和氢氧化钠反应生成盐;亚硫酸根离子能被氧气氧化生成硫酸根离子;
(2)为准确称量固体的质量,在称量之前需洗涤和干燥;
(3)为减少实验误差,最后使完全转化成SO42-,从而完全生成硫酸钡沉淀;双氧水足量时才能将亚硫酸根离子完全转化;
(4)根据一定物质的量浓度溶液的配制中各仪器的作用选取仪器;
(5)根据硫原子守恒计算硫铁矿中硫的质量,从而计算其质量分数.
点评:本题考查了探究物质的含量实验,根据元素化合物的性质来分析解答即可,难度不大,注意为防止空气中二氧化碳的干扰,通入石英管中的空气要先除去二氧化碳,为易错点.

 智能训练练测考系列答案
智能训练练测考系列答案
| |||||||||||||||||||
硫酸渣是用黄铁矿制造硫酸过程中排出的废渣,主要化学成分为SiO2约45%,Fe2O3约40%,Al2O3约10%,MgO约5%。目前我国已经在技术上取得突破——从硫酸渣中分离出各种成分并加以利用。其流程和相关数据如下:

查资料得知:
|
物质名称 |
溶度积(Ksp) |
pH值 |
|
|
开始沉淀 |
完全沉淀 |
||
|
Mg(OH)2 |
5.6×10-12 |
9.3 |
10.8 |
|
Fe(OH)3 |
2.8×10-16 |
2.7 |
3.7 |
|
Al(OH)3 |
1.3×10-33 |
3.7 |
4.7 |
请回答下列问题:
(1)写出固体A的化学式为 。
(2)若要测定溶液的pH是否达到3.7,下列实验用品中可选用的是 。
A.石蕊试液 B.广泛pH试纸 C.精密pH试纸 D.pH计
(3)完成下列离子反应方程式
①溶液D生成固体E ; ②溶液F生成固体G 。
(4)要将固体C、固体E和固体G都转化为相应的稳定氧化物,需进行的实验操作为 。
(5)若不考虑溶液体积的变化,请计算溶液H中c(Mg2+)= 。