题目内容
2.已知某300mLMgCl2与AlCl3的混合液,往其中滴加NaOH溶液,要使沉淀达到最大值,需消耗0.5mol/L的NaOH溶液600mol;则原混合液中c(Cl-)是( )| A. | 0.5mol/L | B. | 0.8mol/L | C. | 1.0mol/L | D. | 1.5mol/L |
分析 MgCl2 与AlCl3的混合液,若往其中滴加NaOH溶液,要使沉淀达到最大值时得到是单一溶质氯化钠,根据组成守恒n(Na+)=n(Cl-),来分析求解.
解答 解:沉淀达到最大值时得到是单一溶质氯化钠,根据组成守恒n(Cl-)=n(Na+)=0.5mol/L×600ml×0.001L/mL=0.3mol,所以混合液中c(Cl-)=$\frac{0.3mol}{0.3L}$=1mol/L,
故选C.
点评 本题考查了镁离子铝离子混合溶液中分离镁离子的方法应用,主要考查沉淀达到最大值时得到是单一溶质氯化钠,根据组成守恒,关键是反应过程的分析判断.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
13.下列用于解释事实的离子方程式书写正确的是( )
| A. | 铁粉溶于氯化铁溶液:Fe+2Fe3+=3Fe2+ | |
| B. | 硫化钠溶液呈碱性:S2-+2H2O?H2S+2OH- | |
| C. | 氯水具有漂白性:Cl2+H2O?2H++Cl-+ClO- | |
| D. | 工业上利用电解饱和食盐水制氯气:2H++2Cl-$\frac{\underline{\;通电\;}}{\;}$H2↑+Cl2↑ |
17.下列各组离子在溶液中因发生氧化还原反应而不能大量共存的是( )
| A. | Ag+、NO3-、Cl-、K+ | B. | K+、Ba2+、OH-、SO42- | ||
| C. | H+、NO3-、Fe2+、Na+ | D. | Cu2+、NH4+、Cl-、OH- |
14.下列说法不正确的是( )
| A. | 液晶态介于晶体状态和液态之间,液晶具有一定程度的晶体的有序性和液体的流动性 | |
| B. | 常压下,0℃时冰的密度比水的密度小,水在4℃时密度最大,这些都与分子间的氢键有关 | |
| C. | 石油裂解、煤的干馏、玉米制醇、蛋白质的变性和纳米银粒子的聚集都是化学变化 | |
| D. | 单质硅是将太阳能转变为电能的常用材料 |
11.日常生活中遇到的很多问题都涉及化学知识,下列有关做法在日常生活中可行的是( )
| A. | 淀粉和纤维素的化学式相同,两者互为同分异构体 | |
| B. | 苯能和氢气发生加成反应,是由于其结构中有碳碳双键 | |
| C. | 紫外线杀菌是在紫外线条件下,蛋白质发生盐析杀死细菌 | |
| D. | 乙醇和乙酸都能与金属钠反应放出氢气 |
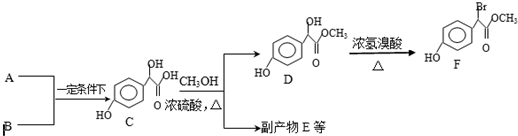
 .
.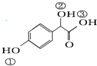 )中①、②、③3个-OH的酸性由强到弱的顺序是:③>①>②.
)中①、②、③3个-OH的酸性由强到弱的顺序是:③>①>②. 任意2种.
任意2种.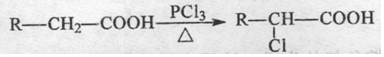 A有多种合成方法,在方框中写出由乙酸合成A的路线流程图(其他原料任选).合成路线流程图示例如下:
A有多种合成方法,在方框中写出由乙酸合成A的路线流程图(其他原料任选).合成路线流程图示例如下: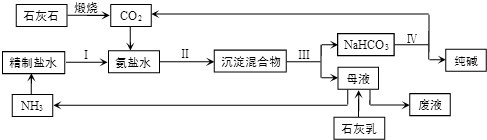
 ;
;